
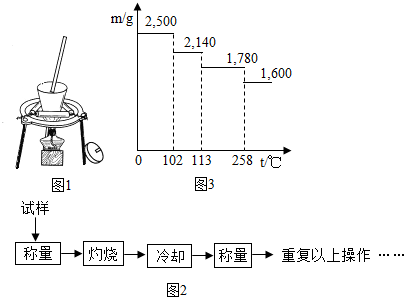
| 加热前质量 | 加热后质量 | |
| m1(容器) | m2(容器+晶体) | m(容器+无水硫酸铜) |
| 5.400g | 7.900g | 7.100g |
分析 (1)根据硫酸铜的化学性质来分析;
(2)根据结晶水合物中,结晶水的质量=m(容器十晶体)-m(容器十无水硫酸铜),据化学方程式可以计算结晶水x的值;
(3)在测定中若被测样品中含有加热挥发的杂质或实验前容器中有水,都会造成测量结果偏高、偏低.
(4)根据CuSO4、结晶水物质的量确定化学式.
解答 解:(1)因为硫酸铜能与水发生化学反应,为了防止硫酸铜吸收空气中的水蒸气,所以必须在干燥皿中进行冷却;故填:硫酸铜能和水反应;
(2)由表格中的数据,硫酸铜晶体的质量为7.9g-5.4g=2.5g,水的质量:7.9g-7.1g=0.8g,
则CuSO 4.xH2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO 4+xH2O,
160+18x 18x
2.5g 0.8g
$\frac{160+18x}{2.5g}=\frac{18x}{0.8g}$
解得x≈4,
故答案为:4;
多次称量可以减少误差,至少称量4次;故填:4;
(3)硫酸铜晶体中,x的值为5,该误差是水测定结果偏小造成的.
a.硫酸铜晶体中含不可能分解的杂质,会导致测定的硫酸铜的质量偏大,测定的水的质量偏小,符合题意;
b.硫酸铜晶体样品未加热完全就开始冷却,会导致测定的硫酸铜的质量偏大,测定的水的质量偏小,符合题意;
c.加热过程中有少量晶体溅出,导致水的质量测定结果偏大,不合题意;
d.加热完毕后,露置在空气中冷却,会造成吸水而导致测定的硫酸铜的质量偏大,测定的水的质量偏小,符合题意;
e.实验前,晶体表面有吸附水,加热后水挥发,而造成加热前后固体的质量差偏大,使x值偏大,不合题意.
故填:abd;
(4)2.500g胆矾的物质的量为2.500g÷250g/mol=0.01mol,其中含结晶水的物质的量为0.05mol;102~113℃之间失去结晶水质量为2.500g-2.140g=0.360g,其物质的量为0.360g÷18g/mol=0.02mol;加热温度在110℃时,剩余固体中CuSO4与结晶水的物质的量之比为0.01mol:(0.05mol-0.02mol)=1:3,故化学式为CuSO4•3H2O,故填:CuSO4•3H2O.
点评 本题考查了实验室测定硫酸铜晶体结晶水含量实验,对失水得到产物的分析判断以及对实验结果产生的误差的原因进行分析是解答的关键,题目难度中等.


科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 往三个集气瓶中分别倒入少量石灰水并振荡 | |
| B. | 燃着的木条分别伸入三集气瓶中 | |
| C. | 用带火星的木条分别放到三个集气瓶瓶口 | |
| D. | 以上三种方法都可以 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | B. | S+O2↑$\frac{\underline{\;点燃\;}}{\;}$SO2 | ||
| C. | H2O═H2↑+O2↑ | D. | 2NaOH+CuSO4═Cu(OH)2↓+Na2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
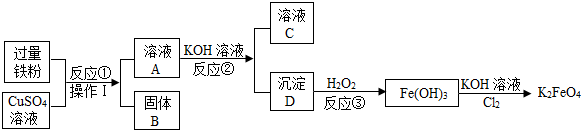
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
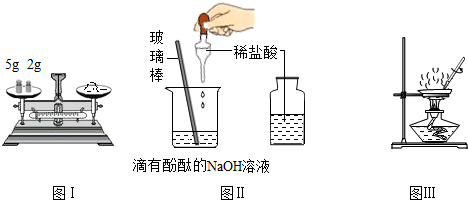
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
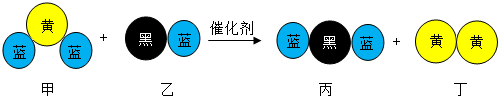
| A. | 乙和丙中所含元素种类相同 | |
| B. | 该反应不可能是置换反应 | |
| C. | 该反应中共有三种元素 | |
| D. | 化学方程式中乙、丁的化学计量数均为1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com