


 智慧小复习系列答案
智慧小复习系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| 实验步骤 | 实验现象 |
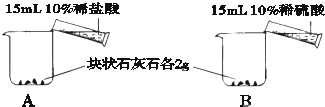 |
A中不断产生气泡,固 体逐渐减少,有少量固体 剩余. B中开始有少量气泡产 生,反应很快停止. |
| 实验步骤 | 实验现象 |
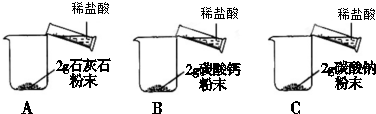 |
A中迅速产生大量 气泡,固体很快减少, 有少量固体剩余. B、C中都迅速产生 大量气泡,固体很快 消失. |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入稀硫酸的质量/g | l0 | l0 | l0 | l0 | l0 |
| 剩余固体质量/g | 8.4 | 6.8 | 5.2 | 3.6 | 3.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:
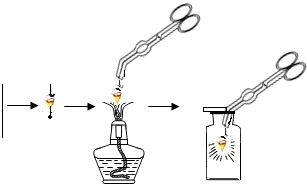
| 物质 | 镁条 | 含碳0.05%铁丝 | 含碳0.2%铁丝 | 含碳0.6%铁丝 |
| 燃烧时的现象 | 剧烈燃烧,发出耀眼 的白光,无火星 |
剧烈燃烧, 极少火星 |
剧烈燃烧, 少量火星 |
(未填) |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 序号 | 实验步骤 | 实验现象 |
| ① | 观察溶液 | 无色液体 |
| ② | 取少量该溶液于试管中,滴加紫色石蕊试液 | 紫色石蕊试液变蓝色 |
| ③ | 另取少量溶液在酒精灯火焰上灼烧 | 火焰呈现黄色 |
| ④ | 取少量该溶液于试管中,先滴加硫酸铜溶液,再滴加稀盐酸 | 先有蓝色沉淀生成,加入稀盐酸后沉淀消失,无其它明显现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:
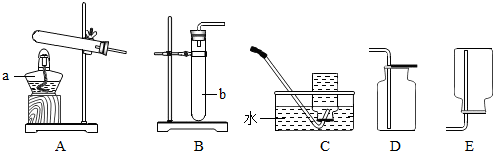
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com