
【题目】下列化学符号中数字表示的意义正确的是()
A.CO2:“2”表示一个二氧化碳分子含有两个氧原子
B.2Na:“2”表示两个钠元素
C.![]() :“+2”表示镁离子带有两个单位的正电荷
:“+2”表示镁离子带有两个单位的正电荷
D.S2-:“2-”表示硫元素的化合价为-2价
科目:初中化学 来源: 题型:
【题目】食盐是生活和工农业生产中最常见的物质之一。晒盐场利用晾晒海水得到粗盐和卤水。
(1)去除粗盐中难溶性的杂质,主要步骤有:溶解、过滤、_________;在过滤操作中,玻璃棒的作用是___________。
(2)在20℃时,向4个盛有200g水的烧杯中,分别加入一定质量的纯净氯化钠固体,并充分搅拌,4组实验数据记录如下
实验序号 | ① | ② | ③ | ④ |
加入氯化钠的质量/g | 9 | 36 | 81 | 90 |
所得溶液的质量/g | 209 | 236 | 272 | 272 |
以下是关于上述实验的叙述,正确的是_______________(填写序号)。
A ①②所得溶液是不饱和溶液
B ③④所得溶液中,溶质的质量分数相等
C 20℃时,200g水中最多可溶解氯化钠的质量为72g
D 20℃时,将④继续恒温蒸发100g水,过滤,得到36g的固体
(3)卤水的主要成分及其溶解度曲线如图,t1℃时:
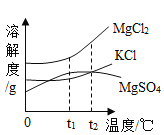
将3种图中物质的饱和溶液升温到t2℃,3种溶液溶质的质量分数由小到大的顺序是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在日常生活中应用广泛。
(1)下列金属制品中,利用金属的导热性的是_____。

(2)我国湿法冶金早在西汉时期就已开始,其中,“曾青得铁则化为铜”便是佐证,即将铁浸入硫酸铜溶液,该反应的化学方程式为_____。
(3)“暖宝宝”中的主要成分是铁粉、氯化钠、活性炭等,其发热原理应用的是铁粉缓慢氧化放热,检验“暖宝宝”是否有效的方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等。综合利用海水制备金属镁的流程如下图所示:
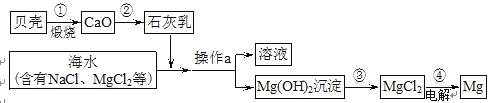
(1)贝壳主要成分的化学式是_________。
(2)操作a的名称是_______,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、_______。
(3)工业冶炼镁常用电解MgCl2的方法,反应为:MgCl2![]() Mg+_____。
Mg+_____。
(4)写出第②、③两步反应的化学方程式:
②___________________,③____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,A~D是初中化学中的四个实验装置,请按要求回答下列问题:
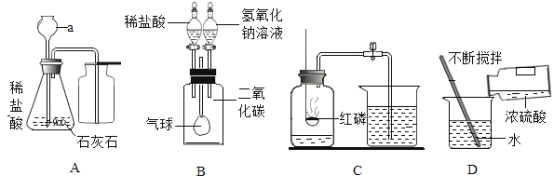
(1)图A中仪器a的名称是_____________;发生反应的化学方程式是________________。
(2)图B是验证CO2与NaOH溶液发生反应的实验,实验的全过程观察到气球的变化情况是_______。
(3)图C是测定空气中氧气含量的实验,实验成功的关键是________________(填字母)。
A 装置的气密性良好 B 装置未冷却时打开止水夹 C 红磷过量或足量
(4)图D是浓硫酸的稀释,实验中玻璃棒的作用是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是几种实验室制取气体的发生装置和收集装置。请回答下列问题:
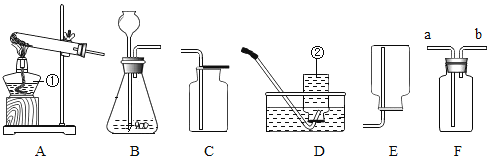
(1)指出图中标有数字的仪器名称:①_____;②_____。
(2)实验室用双氧水和二氧化锰制取氧气时应选用_____(填编号,下同)发生装置,若要收集较为纯净的氧气最好选用_____装置。写出该反应的化学方程式_____;。
(3)实验室用高锰酸钾制取氧气时,发生装置应选用_____(填编号);写出其反应的化学方程式_____;如用F装置收集O2,检验O2是否收集满的方法是_____。
(4)F是一种可用于集气、洗气等的多功能装置,若将F装置内装满水,再连接量筒,就可以用于测定不溶于水且不与水反应的气体体积,则气体应从_____(填“a”或“b”)进入F中。
(5)实验室常用块状电石与水在常温下反应制取难溶于水、密度和空气接近的乙炔气体,根据信息判断:实验室制取乙炔的发生装置应选用_____(填标号,下同),收集装置选用_____。
(6)B装置如果要通过控制滴加液体的速度,来控制反应的程度,可应将长颈漏斗改为_____(填仪器名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】冰箱除味剂是利用活性炭制成的,某化学兴趣小组对冰箱除味剂的性质进行相关探究。
(1)图甲加热装置中发生反应的化学方程式为__________,为了提高加热温度,小组同学用如图的乙装置替代甲装置,你认为提高加热温度的方法还有_________________(答一种即可)。
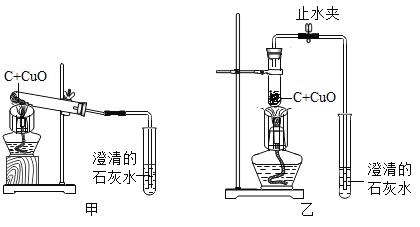
(2)小组同学观察生成的红色固体,发现不同组的实验颜色有差异;为弄清这种红色固体的成分,进行了如下的探究:
[提出问题]反应后的红色固体成分是什么?
[查阅资料]纯净的Cu2O为鲜红色粉末状固体,几乎不溶于水,能与酸溶液发生反应,反应的化学方程式为:![]() 。
。
[猜想与假设]红色固体是:I.Cu II. Cu2O III._______。
[进行实验]
操作 | 现象 | 结论 |
取实验后的红色固体2. 16g于试管中,加入足量稀硫酸充分反应 | __________ | 红色固体定有Cu2O |
[解释与结论]小组内有同学认为猜想II正确,但同学们经过分析后认为这个结论不准确,因为无论红色固体中是否有铜,实验现象都一样,所以猜想II和III都有可能正确。
[反思与评价]要得出正确结论,还需要测定的数据是_______________,若用a表示该数据,则a的取值范围为______________,可以得出猜想III正确。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线:
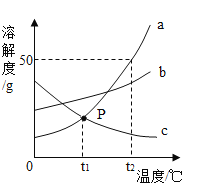
(1)P点的意义是_____;
(2)t2℃时,将50ga物质放入50g水中充分溶解,得到a的溶液的质量为_____g(a物质不含结晶水);
(3)t2℃时,a、b、c三种物质的溶解度由大到小的顺序为:_____;将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是_____;
(4)t2℃时,将c的饱和溶液变为不饱和溶液,可采用_____的方法。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列说法不正确的是( )
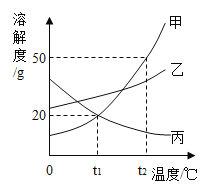
A.t1℃时,甲、丙各20g分别加入100水中,均形成饱和溶液
B.t2℃时,将30g甲物质加入到50g水中不断搅拌,形成的溶液中溶质的质量分数是37.5%
C.将t2℃时甲物质的饱和溶液降温一定析出晶体甲
D.将t2℃时甲、 乙、丙三种物质的饱和溶液降温至t1℃,则三种溶液溶质的质量分数由大到小的关系是:乙>甲>丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com