
| 实验方案 | 实验现象 | 结论 |
| ①取一定量的合金粉末,加过量的 30%NaOH溶液,充分反应后过滤,滤渣备用. ②取步骤①所得滤渣,加过量的10%盐酸,充分反应 | ①粉末部分溶解,并有气体放出. ②滤渣部分溶解,并有气体放出,溶液呈浅绿色 | 合金中一定含有铝、铁、铜三种金属 |
分析 根据题目所给信息,在验证合金中是否有铝时,我们可以利用铝和氢氧化钠溶液反应生成偏铝酸钠和氢气来鉴定.而铁和铜在鉴定时,可以根据铁与氢氧化钠不反应而与盐酸反应,铜两者都不反应来进行了.
解答 解:根据所给的猜想我们可以确定猜想2,可能含有铜.而在检验合金的组成时,可以利用合金中不同的金属的不同化学性质和所给的信息来进行了鉴定.检验是否含有铝时,用氢氧化钠和铝反应生成氢气来确定.而检验是否有铁时,可用稀盐酸来检验.检验是否有铜时,利用铜和稀盐酸不能反应来进行.
故答案为:【实验探究】
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的30%的氢氧化钠溶液,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有 铝. |
| ②取步骤①所得滤渣,加过量的10%盐酸,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有铁和铜. |
点评 原来我们学习碱的性质时,碱不与活泼金属反应,而从所给的信息中,我们知道铝可以和氢氧化钠反应,所以这要求我们在运用知识时,不能盲目的运用所学知识,要根据所题目的意境来解决题目.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质的描述 | 备选物质 |
| ①我能让气球飞起来,却不能燃烧 | A.盐酸 |
| ②我是常见的建筑材料,却害怕高温 | B.氢氧化钠 |
| ③我是常见的调味品,可来自广阔的海洋 | C.氦气 |
| ④我可用于清洗铁锈,是胃酸的主要成份 | D.石灰石 |
| ⑤我被称为新型燃料,燃烧产物对环境无害 | E.食盐 |
| ⑥我在空气中易吸水,溶于水时放热 | F.氢气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 反应后的质量(g) | 17 | m | 6 | 11 |
| A. | 物质Y可能是该反应的催化剂 | B. | 该反应为化合反应 | ||
| C. | 反应中Z和X的质量比为3:2 | D. | 反应的Z和W的质量比为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的30%的氢氧化钠溶液,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有铝. |
| ②取步骤①所得滤渣,加过量的10%盐酸,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有铁和铜. |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
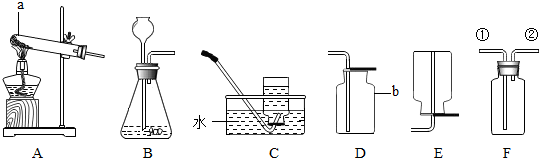
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质类别 | 式量最小的氧化物 | 酸 | 碱 | 盐 |
| 物质化学式 | H2O | H2CO3 | Mg(OH)2 | MgCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 小军见到一种“化学爆竹”(见图)只要用手拍打锡纸袋,掷在地上,锡纸袋随后就会突然爆开并伴随响声.他认为,这是锡纸袋中的物质发生化学反应生成气体造成的,于是想探究锡纸袋中的物质成分.
小军见到一种“化学爆竹”(见图)只要用手拍打锡纸袋,掷在地上,锡纸袋随后就会突然爆开并伴随响声.他认为,这是锡纸袋中的物质发生化学反应生成气体造成的,于是想探究锡纸袋中的物质成分.| 主要实验装置 | 主要操作步骤 | 主要实验现象 | 实验操作目的 |
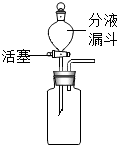 | 在瓶中加入少量白色固体,再加入适量水,振荡,静置 | 白色固体溶解 | 验证白色固体 是否可溶 |
| ①在分液漏斗中加入稀盐酸.塞上胶塞,打开活塞,放出适量溶液后,关闭活塞. ②将气体通入澄清石灰水 | ①大量气泡产生 ②澄清石灰水变浑浊 | 验证生成气体的成分 | |
| 实验的初步结论:白色固体是可溶性碳酸盐,可能为碳酸钠或碳酸氢钠. | |||
| 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com