
【题目】下列实验操作正确的是( )
A. 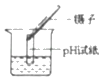 测定溶液的pHB.
测定溶液的pHB. 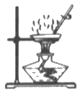 蒸发结晶
蒸发结晶
C.  点燃酒精灯D.
点燃酒精灯D. 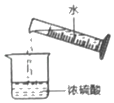 稀释浓硫酸
稀释浓硫酸
科目:初中化学 来源: 题型:
【题目】为测定标有质量分数为32%的盐酸的实际质量分数,小明实验时先在烧杯中加入20 g 40%的氢氧化钠溶液,再逐滴加入该盐酸,测定出加入盐酸的质量与烧杯中溶液pH的关系如图。
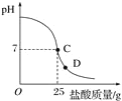
(1)所用氢氧化钠溶液中溶质的质量为_____g。
(2)请认真看清上图信息后回答以下问题。
①当滴加盐酸到C点时,所消耗的盐酸中溶质的质量是多少?_____。
②该盐酸的实际质量分数是多少?(保留到0.1%)_____。
③导致盐酸溶液的溶质质量分数改变的原因是_____。
④当滴加盐酸到图像中D点时,烧杯中溶液的溶质是_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(9分)张华同学对酸、碱、盐的知识进行了以下的梳理。
(1)填写下表空格中的化学式。
氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
KCl | CaCl2 | NaCl | MgCl2 | ZnCl2 | FeCl2 |
思考:根据以上盐中的金属元素的排列,可以得出他是依据______________顺序归纳整理的。
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图。请你在右边的圆圈中填入适当的化学式或离子符号:

(3)张华同学发现酸、碱、盐之间的反应都有盐类物质生成。请写出一个能生成MgCl2的复分解反应的化学方程式:__________________________。
(4)我们知道溶液酸碱度pH可显示的溶液的酸碱性;酸溶液pH<7,溶液显酸性;碱溶液pH>7,溶液显碱性.提出问题:盐溶液的pH怎样呢?盐溶液显什么性呢?
猜想与假设:盐溶液的pH可能为:pH=7、pH<7、pH>7.
设计与实验:下列是两同学分别对相同的NaCl溶液、CuSO4溶液、K2CO3溶液的pH进行的测定实验:甲同学:取pH试纸放在玻片上,用玻棒蘸取测试液滴在pH试纸上,试纸显色后与pH标准比色卡比较.乙同学:取pH试纸放在玻片上,用蒸馏水将pH试纸润湿,再用玻棒蘸取测试液滴在pH试纸上,试纸显色后与pH标准比色卡比较.
记录数据:下表是两同学记录所测pH的实验数据:
NaCl溶液 | CuSO4溶液 | K2CO3溶液 | |
甲同学 | 7 | 4 | 10 |
乙同学 | 7 | 5 | 9 |
结论:通过测定几种盐溶液的pH,可以得出的结论是: .
评价与反思:上述两同学测得的数据,反映了溶液真实pH的是 同学。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验操作,能达到预期目的是
①用托盘天平称取5.6gCuO粉末
②用10mL水和10mL酒精配制20mL酒精溶液
③将50g溶质质量分数为10%的稀盐酸加热蒸发掉25g水,得到溶质质量分数为20%的盐酸
④用10mL的量筒取8.2mL水
A.①③④ B.①④ C.①②④ D.②③
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】近些年来,我国的高铁技术飞速发展。结合所学化学知识,回答下列问题:

(1)图中标示的物质中为金属材料的是______(填序号)。
(2)动车电路中的导线大多是用铜制的,这是利用了铜的延展性和______性。
(3)动车表面喷漆主要是为了防止外壳生锈,其原理是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学常从宏观和微观角度研究、认识物质。
(1)以下是用新型催化剂将二氧化碳转化为汽油的三个环节。(a、b是两种起始反应物的分子结构,c、d是制得的汽油中所含物质的分子结构)请回答下列问题:
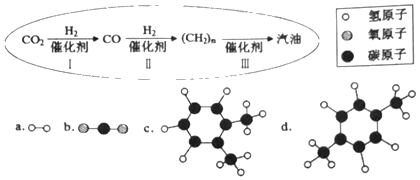
①环节I的转化中,碳元素化合价的变化为_____。
②试写出c物质的化学式_____,认真观察c和d两种物质的分子结构模型,可知c和d不是相同物质,原因是_____。
③“二氧化碳变汽油”的研究成果,使我国成为此领域的世界领跑者。请你写出一点该成果的现实意义_____。
(2)碳酸钙与氧化钙的混合物中,钙元素的质量分数为50%,取该混合物16g,经过高温煅烧后,将剩余固体投入足量水中,固体全部溶解成氢氧化钙。
①固体投入足量水中发生反应的化学方程式_____,属于_____反应(填基本反应类型)。
②生成氢氧化钙的质量为_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~G是初中化学常见的物质。己知A、C组成元素相同,均为无色气体;B为红棕色粉末;F为黑色金属氧化物,A跟F的反应与A跟B的反应类型相似。它们的转化关系如下图所示,下列推断错误的是 ( )

A. 若A是CO,则B是Fe2O3
B. 若B是Fe2O3,则G一定是Fe2(SO4)3
C. 反应II的化学方程式是:CO2+C![]() 2CO
2CO
D. 反应III的化学方程式是:Fe+CuSO4=FeSO4+Cu
查看答案和解析>>
科目:初中化学 来源: 题型:
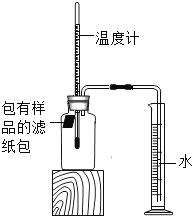
【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表。
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
3 | …… | 100 | 70 | 约480 |
(1)实验①和②说明NaCl可以_____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____。
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____(小数点后保留1位)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国制碱工业的先驱侯德榜发明了“侯氏联合制碱法”,其模拟流程如下,下列说法错误的是
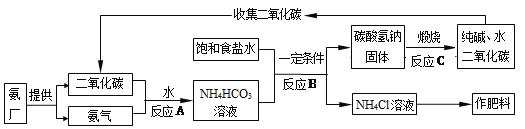
A. 反应A B C中不涉及的基本反应类型是置换反应
B. 反应B的反应方程式是:NaCl+NH4HCO3=NaHCO3↓+NH4Cl
C. “侯氏联合制碱法”的主要产品“碱”是指碳酸氢钠
D. 该模拟中能循环利用的物质是二氧化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com