
【题目】乙烯(C2H4)是一种果实催熟剂。下列有关叙述正确的是
A. 1个乙烯分子中含有6个原子
B. 乙烯是由2个碳元素和4个氢元素组成的
C. 乙烯中氢元素的质量分数最大
D. 乙烯中碳、氢元素的质量比1:2
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:初中化学 来源: 题型:
【题目】下列有关实验现象的描述中,不正确的是( )
A. 木炭在氧气中燃烧发出白光
B. 硫粉在空气中燃烧产生蓝紫色火焰
C. 二氧化碳不断通入紫色石蕊溶液中,溶液由紫色变为红色
D. 打磨后的铝片放入硫酸铜溶液中,铝片表面出现红色固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式表示的反应正确,且能实验目的是( )
A.高炉炼铁:2Fe2O3+3C![]() 4Fe+3CO2↑
4Fe+3CO2↑
B.湿法炼铜:2Fe+3CuSO4=Fe2(SO4)3+3Cu
C.天然气作燃料:CH4+O2![]() CO2+2H2O
CO2+2H2O
D.实验室用加热氯酸钾制取氧气:2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊。甲组同学进行右图所示的实验,却未观察到预期现象。

【提出问题】未观察到浑浊的原因是什么?
【猜想和假设】
①与氢氧化钙溶液的浓度有关。若使用更大浓度的氢氧化钙溶液,会迅速产生浑浊。
②与碳酸钠溶液的浓度有关。若使用更大浓度的碳酸钠溶液,会迅速产生浑浊。经讨论,同学们认为猜想①不合理,其理由是 。
【进行实验】乙组同学针对猜想②进行实验。
实验目的 | 实验操作 | 实验现象 | |
探究猜想② | 取4支试管,向其中分别加入 | 碳酸钠溶液浓度/% | 是否浑浊 |
10 | 不浑浊 | ||
5 | 不浑浊 | ||
1 | 浑浊 | ||
0.5 | 浑浊 | ||
【解释与结论】
(1)补全上述实验操作:取4支试管,向其中分别加入 。
(2)氢氧化钙溶液与碳酸钠溶液混合出现浑浊的化学方程式是 。
(3)乙组实验证明:猜想②不成立,碳酸钠溶液浓度在0.5~10%的范围内,能否出现浑浊与碳酸钠溶液的浓度有关,其关系是 。
【实验反思】
(1)丙组同学对乙组所做实验中未出现浑浊的原因进行探究。设计了多组实验,其中部分同学的实验过程及结果如下:

丙组同学的实验目的是 。
(2)依据乙、丙两组的实验探究,丁组同学仍使用甲组的仪器和药品对甲组实验进行了改进,当滴入几滴某溶液后,溶液迅速变浑浊。其实验操作是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某校同学开展了“燃烧的条件”的探究活动.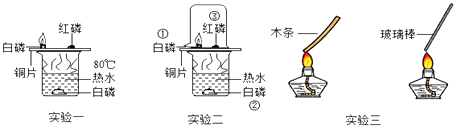
(1)实验二与实验一相比,其优点是 , 实验一和实验二在烧杯上放了一块薄铜片,主要利用了铜具有良好的性.
(2)对照实验二中①和③能够获得可燃物燃烧需要的条件之一是 . 实验三能说明燃烧需要的条件之一是 , 实验三完毕,熄灭酒精灯的操作是 .
(3)从实验一中观察到的现象及所得到的结论正确的是__________
A.实验中烧杯里的热水只起提高温度的作用
B.水下白磷未燃烧是由于没有与氧气接触
C.实验说明可燃物燃烧时必须满足的条件是温度达到着火点或与氧气接触
D.白磷的着火点低于80℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用加热高锰酸钾并用排水法收集氧气,下列做法或说法正确的是 ( )
A. 在试管口放一团棉花,目的是防止高锰酸钾粉末进入导管
B. 点燃酒精灯后,将外焰直接对准固体药品部位加热
C. 导管口刚有气泡冒出时,就立即开始收集气体
D. 实验结束时,先熄灭酒精灯,再将导管从水槽中移出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组在调查市场时发现下列一些现象,他们所提建议中不正确的是
A.海鲜在夏天容易腐烂变质,建议用甲醛溶液浸泡海鲜防腐
B.羊毛纤维和合成纤维外观不好鉴别,建议生活中用燃烧法鉴别
C.废旧电池随意丢弃对环境有污染,建议将其回收并集中处理
D.蔬菜饼干易氧化变质,建议包装时加入一小包铁粉作抗氧化剂和吸水剂并密封
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】析处理图表中的信息是学习化学的一种重要方法,CO2可与NaOH溶液反应生成Na2CO3和H2O.NaOH、Na2CO3、NaCl在不同溶剂中的溶解度如表所示.
物质 | 不同温度下在水中溶解度(S/g) | 常温下在乙醇中的溶解度(S/g) | |||
0℃ | 10℃ | 20℃ | 30℃ | ||
NaOH | 42 | 51 | 109 | 119 | 17.3 |
Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 | <0.01 |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 0.1 |
根据表中数据回答下列问题:
(1)NaOH在水中的溶解度随温度升高而 (填“增大”或“减小”);
(2)请用相应的数据列式表示20℃时饱和食盐水中溶质的质量分数为 (不要求计算结果);
(3)请写出一种把Na2CO3的不饱和溶液变为饱和溶液的方法 ;
(4)为证明CO2能与NaOH发生反应,小明同学将CO2通入饱和NaOH的乙醇溶液中.请推测该实验可观察到的现象 ,推测依据是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com