
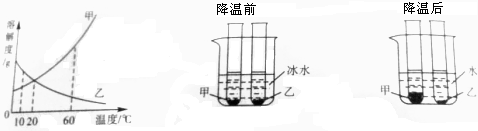
分析 常温下物质的饱和溶液(试管底部均有未溶解的固体)放进盛有冰水的烧杯里,操作的目的是对饱和溶液进行降温;然后根据物质的溶解度曲线图,对溶液的溶质质量分数、剩余固体的质量、物质的溶解度等的变化情况进行分析.
解答 解:甲物质的溶解度曲线表明,温度降低物质的溶解度减小,所以,放入冰水后,随温度降低甲物质的溶解度变小,试管内饱和溶液析出晶体,底部固体物质甲增加;则甲物质的质量分数也会减小;
乙物质的溶解度曲线表明,温度降低物质的溶解度变大,所以,放入冰水后,随温度降低乙物质的溶解度变大,试管底部固体物质乙继续溶解,则乙溶液剩余的固体减少,乙物质的质量分数会增大;
当降温到20℃时,甲物质的溶解度变小,试管内饱和溶液析出晶体,从图看出乙溶液试管底部有未溶解的固体,为饱和溶液,两种物质的溶解度相等,所以甲溶液的浓度等于乙溶液的浓度;所含溶质质量相等;
当降温到10℃时,甲物质的溶解度变小,试管内饱和溶液析出晶体,从图看出乙溶液试管底部有未溶解的固体,为饱和溶液,甲的溶解度小于乙的溶解度,所以甲溶液的浓度小于乙溶液的浓度;
故答案为:减小;增大;等于;等于;小于.
点评 本题考查了对溶解度曲线的理解;从溶解度曲线不仅能看出物质溶解度随温度的变化情况,还能看出不同物质在不同温度时溶解度的大小等;要掌握固体物质的溶解度只受外界温度的影响.


科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝伸入盛有氧气的集气瓶中剧烈燃烧,火星四射,生成黑色固体 | |
| B. | 磷在空气中燃烧,反应剧烈,产生大量白烟 | |
| C. | 镁带在空气中燃烧,发出耀眼白光,生成白色固体 | |
| D. | 硫在氧气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
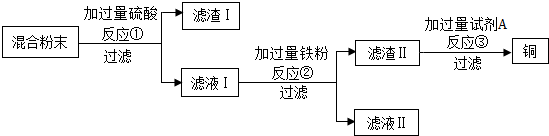
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
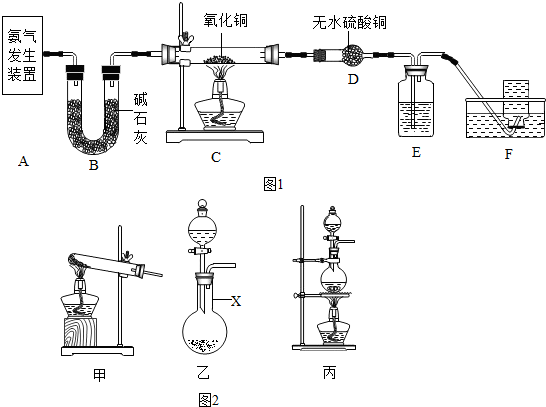
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
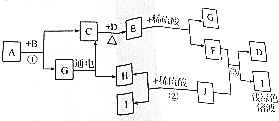 A一J是初中化学常见物质,A、G由相间的元素组成,常温下均为无色液体.B、E为黑色固体,D、J为金属单质,I为浅绿色溶液,这些物质的相互转化关系如图所示.
A一J是初中化学常见物质,A、G由相间的元素组成,常温下均为无色液体.B、E为黑色固体,D、J为金属单质,I为浅绿色溶液,这些物质的相互转化关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)
某白色固体A可能含有碳酸钠、硫酸钠、氯化钠、硝酸钡中的一种或几种,进行如下实验:(信息提示:硫酸钠、硝酸钡溶液呈中性)| 实验操作 | 现象 | 结论 |
| 取滤液C少量,滴入足量Ba(NO3)2溶液;过滤后往滤液中滴入AgNO3溶液 | 产生白色沉淀 | 确定A固体中还含有氯化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 同学们在探究物质燃烧的条件时,设计了如图所示的实验,请回答有关问题.
同学们在探究物质燃烧的条件时,设计了如图所示的实验,请回答有关问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com