
| A. | 盐酸 | B. | 纯碱 | C. | 干冰 | D. | 氢氧化钙 |
科目:初中化学 来源: 题型:多选题

| A. | 该反应是化合反应 | |
| B. | 反应前后原子的种类、个数都不变 | |
| C. | 甲和丙两种物质的质量比为11:4 | |
| D. | 甲乙丙三种物质的分子数比为1:1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
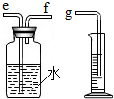 “寒假假期”,小兵对“铁与稀硫酸反应快慢的影响因素”进行了探究.
“寒假假期”,小兵对“铁与稀硫酸反应快慢的影响因素”进行了探究.| 实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
| 实验 编号 | 试剂 | 前10min内产生的 氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30mL30% | 564.3 |
| b | 含杂质的锌 | 30mL30% | 634.7 |
| c | 纯锌 | 40mL30% | 449.3 |
| d | 纯锌 | 40mL30% | 602.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
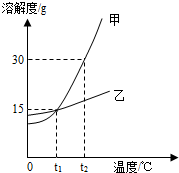 如图是甲、乙两物质的溶解度曲线,下列说法正确的是( )
如图是甲、乙两物质的溶解度曲线,下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t1℃时甲、乙两物质的饱和溶液中的溶质的质量分数均各15% | |
| C. | 将接近饱和的甲溶液升高温度可变为饱和溶液 | |
| D. | t2℃时,将相同质量的甲、乙两种物质分别配成饱和溶液,得到的溶液质量乙>甲 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
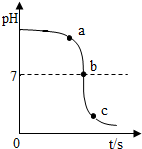 某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,通过数字化传感器测得烧杯中溶液pH值的变化图象如图所示.下列说法正确的是( )
某校化学小组在利用稀硫酸和氢氧化钠溶液探究酸碱中和反应时,通过数字化传感器测得烧杯中溶液pH值的变化图象如图所示.下列说法正确的是( )| A. | 图中a点所示溶液呈酸性 | |
| B. | 图中b点所示溶液中主要含有两种离子 | |
| C. | 图中c点所示溶液中含有的溶质是Na2SO4和NaOH | |
| D. | 该实验是将氢氧化钠溶液逐滴滴入到盛有稀硫酸的烧杯中 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
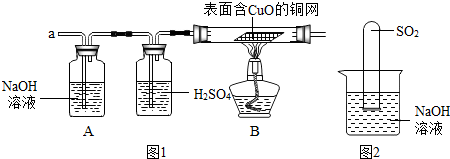
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子在化学反应中可分,则原子在化学反应中也可分 | |
| B. | 水电解产生氢气和氧气,所以水是由氢气和氧气组成的 | |
| C. | 氧化物中一定含有氧元素,但含氧元素的化合物不一定是氧化物 | |
| D. | 二氧化锰是加快过氧化氢分解的催化剂,所以催化剂都能加快化学反应的速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com