
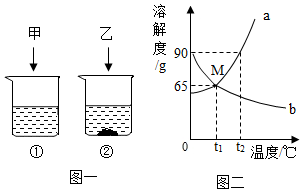
 t2℃时,将甲、乙各80g分别放在盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一,甲和乙的溶解度曲线如图二.请结合图示回答下列问题:
t2℃时,将甲、乙各80g分别放在盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一,甲和乙的溶解度曲线如图二.请结合图示回答下列问题:分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)t2℃时,将甲、乙各80g分别放在盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,甲固体全部溶解,乙固体有剩余,所以t2℃时,甲物质的溶解度大于乙物质的溶解度,固体甲对应的溶解度曲线是a;
(2)M点的含义是:t1℃时,甲、乙物质的溶解度相等;
(3)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分甲析出,“全部溶解”的原因是:甲物质溶于水放热,温度升高,溶解度增大;
(4)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,乙物质会析出晶体,甲物质不会析出晶体,所以
a.甲溶液仍为饱和溶液,故正确;
b.两溶液质量甲<乙,故正确;
c.t2℃时,甲物质的溶解度大于乙物质的溶解度,所以等质量的甲、乙饱和溶液中,甲的溶剂质量小于乙,所以降温后,两溶液中溶剂质量不相等,故错误;
d.甲物质t1℃时的溶解度大于乙物质t2℃时的溶解度,所以两溶液溶质质量分数甲>乙,故正确.
故选:abd.
故答案为:(1)a;
(2)t1℃时,甲、乙物质的溶解度相等;
(3)甲物质溶于水放热,温度升高,溶解度增大;
(4)abd.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 用稀盐酸除铁锈 Fe2O3+6HCl═2FeCl2+3H2O 复分解反应 | |
| B. | 石笋、石柱的形成 CaCO3+H2O+CO2═Ca(HCO3)2 化合反应 | |
| C. | 用含氢氧化镁的药物治疗胃酸过多症:Mg(OH)2+2HCl=MgCl2+2H2O 复分解反应 | |
| D. | 证明锌比银活泼 Zn+2AgCl═ZnCl2+2Ag 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用小苏打除去面团发酵产生的酸 | B. | 用白醋长时间浸泡铝壶内的水垢 | ||
| C. | 用食盐除去铁锅内的油污 | D. | 用燃着的火柴检查煤气罐是否漏气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
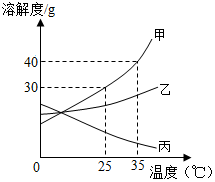 甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
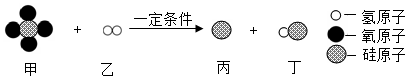
| A. | 甲物质由5个原子构成 | |
| B. | 化学变化前后硅元素的化合价不变 | |
| C. | 参加反应的乙的质量和生成的丁中氢元素的质量相等 | |
| D. | 参加反应的甲、乙两种物质的分子个数比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
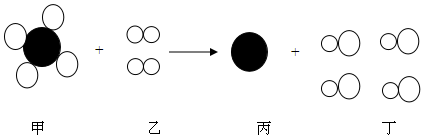
| A. | 该反应属于复分解反应 | B. | 1个甲分子由5个原子组成 | ||
| C. | 该示意图中共有2种化合物分子 | D. | 反应中乙、丁两物质的质量比为1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com