
分析 根据物质的性质进行分析,酚酞试液在碱性溶液中为红色,在酸性和中性溶液中为无色,盐酸能与碱发生中和反应,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠.
解答 解:样品溶于水加入酚酞试液为无色,说明溶液中不含有碱性物质,所以溶液的组成是:盐酸、氯化钠溶液;
取适量样品放入试管中,滴加无色酚酞溶液,溶液变成红色,说明溶液呈碱性,可能是氢氧化钠和碳酸钠溶液,也可能是氢氧化钙和氢氧化钠溶液,再向试管中加入过量的氢氧化钙溶液,观察到有沉淀产生,则溶液中一定含有碳酸钠,碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,为确定样品组成,取适量样品放入试管中,滴加过量的硝酸钙溶液,过量的硝酸钙能将溶液中含有的碳酸钠反应生成碳酸钙沉淀和硝酸钠,若加入酚酞试液溶液变红,则样品中含有氢氧化钠,若加入酚酞试液不变色,则样品中含有氯化钠.
故答案为:
(1)盐酸、氯化钠溶液.
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH; Na2CO3,Ca(OH)2、NaOH;
(3)无色酚酞,氢氧化钠.
点评 在解此类题时,首先分析所给混合物中各物质的性质,然后根据题中所给的实验现象进行判断,最后确定混合物的组成成分.


科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验桌上酒精着火立即用水浇灭 | |
| B. | 实验室制取氯化氢气体时,用排水法收集 | |
| C. | 测定溶液酸碱度时,将pH试纸直接放入待测液中 | |
| D. | 配制稀硫酸时,将浓硫酸倒入水中,并用玻璃棒不断搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
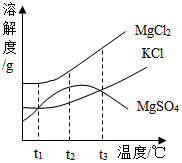
| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 |
| 溶解度/g | 36.0 | 21.6 | 37.2 | 9.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
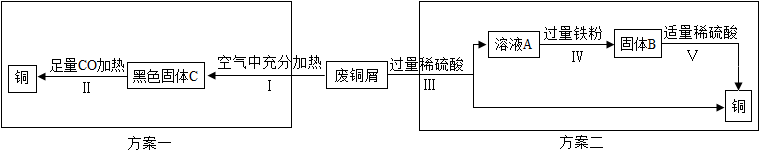
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
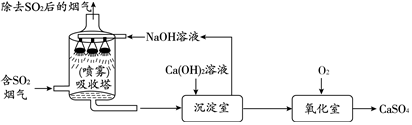
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.90 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com