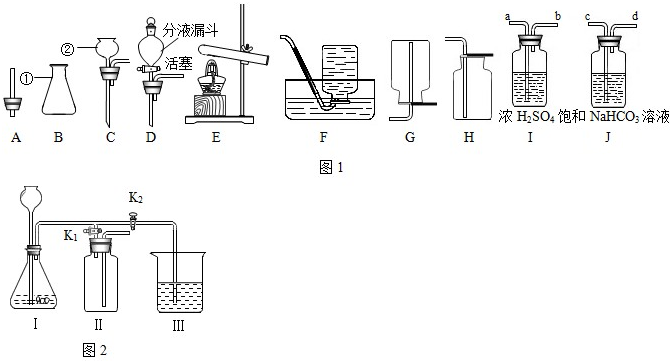
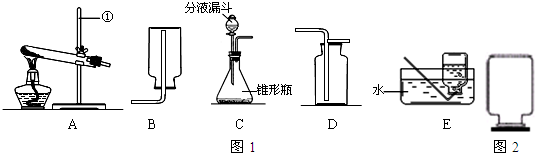
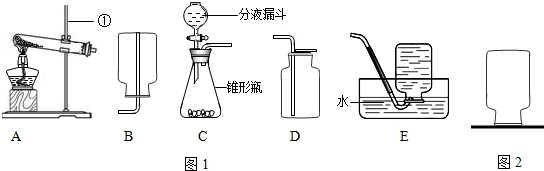
解:(1)编号①是锥形瓶;
(2)用加热氯酸钾的方法制取氧气,属于固体加热型,选择E装置,氧气导出还要用到单孔塞A,氧气不易溶于水,故收集较纯净的氧气用排水法,方程式是2KClO
3
2KCl+3O
2↑;二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水,方程式是2NaOH+SO
2=Na
2SO
3+H
2O;
(3)实验室用大理石和稀盐酸反应制取二氧化碳,属于固液常温型,控制反应速率可用分液漏斗,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集,据此选择仪器BDH,反应方程式是CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;除去氯化氢气体用饱和的碳酸氢钠溶液,除去水蒸气用浓硫酸,洗气装置中导管要长进短出,除水蒸气放于后面,防止碳酸氢钠溶液中水蒸气的干扰;
(4)①当打开K
1、关闭K
2时,利用I、Ⅱ装置,可用于固液混合常温制取气体,且气体的密度比空气小,二氧化碳的密度比空气大,故不能用来制取二氧化碳;
②二氧化碳与水反应生成碳酸,碳酸可使石蕊试液变红,所以若要证明二氧化碳能与水发生反应,应向烧杯的水中加入石蕊试液;
故答案为:(1)锥形瓶;
(2)AEF; 2KClO
3
2KCl+3O
2↑;2NaOH+SO
2=Na
2SO
3+H
2O;
(3)BDH;CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑; cdab
(4)①b; ②石蕊试液.
分析:(1)据常用仪器回答;
(2)用加热氯酸钾的方法制取氧气,属于固体加热型,选择E装置,氧气导出还要用到单孔塞A,收集较纯净的氧气用排水法,据反应原理书写方程式;二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水,据此书写方程式;
(3)实验室用大理石和稀盐酸反应制取二氧化碳,属于固液常温型,控制反应速率可用分液漏斗,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集,据此选择相关仪器,书写反应方程式;除去氯化氢气体用饱和的碳酸氢钠溶液,除去水蒸气用浓硫酸,洗气装置中导管要长进短出,除水蒸气放于后面,防止干扰;
(4)①当打开K
1、关闭K
2时,利用I、Ⅱ装置,可用于固液混合常温制取气体,且气体的密度比空气小;
②若要证明二氧化碳能与水发生反应,应向烧杯的水中加入石蕊试液,酸性溶液可使石蕊试液变红.
点评:据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,此外,掌握气体的性质、制取氧气、二氧化碳的反应原理等并会灵活应用是解答问题的关键因素.


 2KCl+3O2↑;二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水,方程式是2NaOH+SO2=Na2SO3+H2O;
2KCl+3O2↑;二氧化硫和氢氧化钠溶液反应生成亚硫酸钠和水,方程式是2NaOH+SO2=Na2SO3+H2O; 2KCl+3O2↑;2NaOH+SO2=Na2SO3+H2O;
2KCl+3O2↑;2NaOH+SO2=Na2SO3+H2O;