
【题目】化学用语是学习化学的重要工具,是国际通用语言,请用适当的化学用语填空。
(1)由3个氧原子构成的单质分子:_______;
(2)两个硝酸根离子:_________;
(3)氯酸钾中氯元素的化合价:_________;
(4)氖气:_________;
(5)三个五氧化二磷分子:_________。
【答案】O3 ![]()
![]() Ne 3P2O5
Ne 3P2O5
【解析】
(1)元素符号右下角的数字表示几个原子构成一个分子,由3个氧原子构成的单质分子是臭氧分子,化学式为O3;
(2离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其元素符号前加上相应的数字,故两个硝酸根离子可表示为:![]() ;
;
(3) 由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,氯酸钾中钾元素化合价为+1,氧元素化合价为-2,根据化合物各元素化合价代数和为0,氯元素为+5价,故氯酸钾中氯元素的化合价可表示为:![]() ;
;
(4) 氖气为原子直接构成的单质,所以化学式为Ne;
(5) 一个五氧化二磷分子是由2个磷原子和5个氧原子构成的,表示多个该分子,就在其化学式前加上相应的数字,五氧化二磷分子的前面加3表示三个五氧化二磷分子:3P2O5。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:初中化学 来源: 题型:
【题目】向盛有稀盐酸的烧杯中逐滴加入NaOH溶液,测得烧杯中溶液的pH变化如图所示,下列说法正确的是
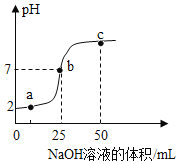
A.a点所示的溶液中含有的溶质是NaOH和NaCl
B.b点所示的溶液能使紫色石蕊溶液变红
C.c点表示NaOH和稀盐酸恰好完全反应
D.a、b、c所示的溶液中溶质都含有NaCl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据部分原子结构示意图,请回答:
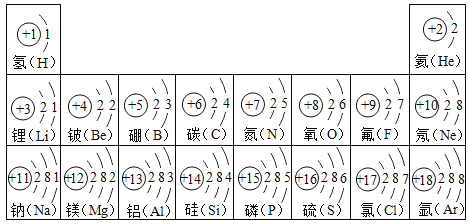
(1)氧元素和硫元素化学性质相似的原因是_____________________;
(2)根据氟原子、钠原子的结构特点,判断构成氟化钠的粒子符号是___________;
(3)同一周期(横行)的原子结构具有共同的特点是_________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室提供下列仪器:
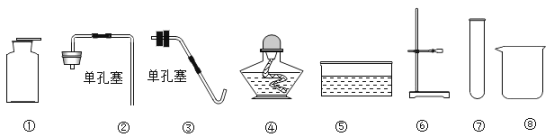
(1)用石灰石和稀盐酸制得CO2并观察CO2与石蕊溶液反应的现象,所需仪器按组装顺序依次是_____(填序号),发生化合反应的化学方程式是_____。
(2)用氯酸钾和二氧化锰制取O2,所需仪器按组装顺序依次是____(填序号),反应的化学方程式是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙是初中化学常见的三种物质,其相互转化关系如图,通常甲为固态单质,乙、丙为常温下的两种常见气体,且所含元素种类相同,乙易与血液中的血红蛋白结合。下列说法正确的是( )
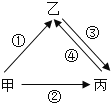
A.①②两个转化的反应中,只能验证甲具有可燃性
B.干燥的丙能使紫色石蕊变成红色
C.③的转化可通过和金属氧化物反应来实现
D.乙和丙均由分子构成,且都易溶于水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国是世界化肥第一生产大国和消费大国。以空气和煤炭等为化工原料,可合成氨、尿素(CO(NH2)2),主要生产工艺流程如下图所示。回答下列问题:
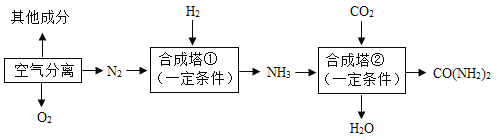
(1)工业合成氨的原料是氮气和氢气,氮气可从空气分离中获得。从液态空气中分离出N2的过程属于____(填“物理”或“化学”)变化。空气中含量少量的稀有气体,其化学性质极为_____(填“活泼”或“稳定”)。
(2)氢气通过煤和水蒸气在高温时反应得到的合成气(H2、CO)提取,制备合成气前需先将煤粉碎,这样做的目的是_____,反应的基本类型为________。
(3)写出合成塔①中合成氨的化学方程式为________。尿素属于_____(填“氮”“钾”“磷”或“复合”)肥。
(4)压强为101kPa下,氨气在不同温度下的溶解度如下表。氨水是氨气的水溶液,贮存时氨水要注意_____。
温度/℃ | 10 | 20 | 30 | 60 |
溶解度/g | 70 | 56 | 44.5 | 20 |
(5)2019年全国节能宣传周主题为“绿色发展,节能先行”。其中符合要求的___(填序号)
A 烟囱中排放出未经处理的烟尘、废水和废气
B 综合采用煤的洁净化技术
C 循环利用氮气、氢气和水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学变化通常伴随有能量的变化,其原因是单质和化合物内部都存在有一种能量,即化学能。近年来,研究人员提出利用含硫物质热化学循环实现太阳能的储存与转化。过程如下:
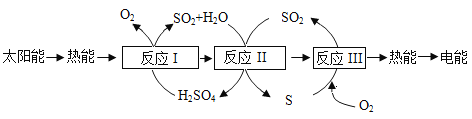
在反应Ⅰ、Ⅱ、Ⅲ中,反应物和生成物均得以循环利用。如反应Ⅱ是反应Ⅰ生成的SO2、H2O及反应Ⅲ生成的SO2发生反应生成H2SO4和S。
(1)在这一方案中,太阳能以_______能的形式储存下来。
(2)反应Ⅰ的化学反应方程式是______________。
(3)反应Ⅲ属于基本反应类型中的________反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学对氢化钙(CaH2)的制备和性质进行了如下探究:
(阅读资料)
①H2与钙加热可制得CaH2;
②钙和氢化钙都能和水反应,生成物都是一种碱和一种气体。
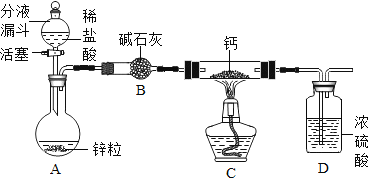
(实验探究)设计的制取装置如图所示:
(1)碱石灰的主要成分为氧化钙和氢氧化钠,装置B的作用是_______;根据完整的实验装置进行实验,实验步骤如下:检查装置气密性、装入药品、打开分液漏斗活塞,此后的实验步骤正确的顺序是____(填序号)。
A 加热反应一段时间
B 收集装置最右端导管口处的气体并检验其纯度
C 关闭分液漏斗活塞
D 停止加热,充分冷却
(2)制备CaH2实验结束后,取少量反应后固体小心加入水中,观察到有气泡产生,在溶液中滴入酚酞试液后显______色。该同学据此判断:实验中确有氢化钙生成,其他同学认为他的结论不一定正确,原因是_______。
(3)取少量上述制得的CaH2样品加到足量的碳酸钠溶液中,产生大量气泡,过滤得滤渣和滤液,经检验滤渣的成分是碳酸钙,点燃产生的气体,火焰呈淡蓝色,将该气体的燃烧产物通入澄清石灰水中,无现象,则该气体为______(写化学式)。
(4)对滤液中溶质的成分做出如下猜测并进行实验:
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因:_________。
(实验验证)
实验 | 现象 | 结论 |
实验一:取滤液,向其中滴入少量Na2CO3溶液 | _____ | 猜想二不成立 |
实验二:另取滤液,向其中加入足量稀盐酸 | _____ | 猜想三成立 |
(定量分析)
CaH2可用于冶金工业,还可以作为轻便的氢气发生剂,现有126克纯净的CaH2,加入足量水中,理论上可获得氢气____升?(常温常压下,氢气的密度为0.09g/L,结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】北宋张潜在其《浸铜要略序》一书中对铜的冶炼有如下记载:“山麓有胆泉,土人汲以浸铁,数日辄类朽木,刮取其屑,锻炼成铜”。
(1)书中提及的“胆泉”为硫酸铜溶液,“浸铁”即将铁放入其中,写出此冶炼铜方法中生成铜的化学方程式__。
(2)若“浸铁”前后溶液中存在的离子种类如图所示,其中![]() 表示不同种类的离子,则“
表示不同种类的离子,则“![]() ”表示_____(填写离子符号)。
”表示_____(填写离子符号)。
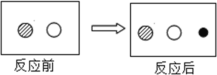
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com