
 铁、铝、铜是日常生活中使用最广泛的金属.
铁、铝、铜是日常生活中使用最广泛的金属.| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
| 密度/(g•cm-3) | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
| 熔点/℃ | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 2.5~3 | 2~2.9 | 2.5 | 4~5 | 1.5 |
分析 (1)分析金属活动性与金属冶炼先后顺序的关系;
(2)根据贴的硬度大和密度大进行解答;
(3)根据金属铝与氧化铜在高温条件下生成铜和氧化铝进行解答;
(4)根据铁的性质进行解答;
(5)根据化学式的意义进行计算.
解答 解:(1)人类最早大规模冶炼和使用的是铜,最晚的是铝,而三种金属的活动性由弱到强的顺序为:铜<铁<铝;由此可发现金属的大规模冶炼和使用与金属活动性有较密切关系:活动性强的金属较晚被冶炼和使用;
(2)碎石用的大锤常用铁制而不用铝制,而对比表中铁、铝的数据可发现:铁的硬度,密度比铝大;
(3)金属铝与氧化铜在高温条件下生成铜和氧化铝,化学方程式为:2Al+3CuO$\frac{\underline{\;高温\;}}{\;}$3Cu+Al2O3;由此我发现了一条新的判断依据:在高温条件下,位于前面的金属能把位于后面的金属从它们的氧化物里置换出来;
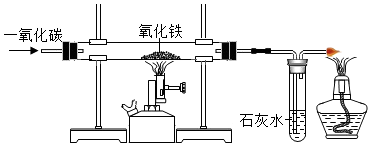
(4)一氧化碳与氧化铁反应生成铁和二氧化碳,所以玻璃管内的粉末由红色变为黑色;该反应的化学方程式为 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2 Fe+3CO2;在此实验中体现一氧化碳具有可燃性、还原性、毒性;
(4)Cu2S中铜元素的质量分数为:$\frac{64×2}{64×2+32}$×100%=80%;
用500吨含Cu2S80%的铜矿石,理论上可以炼出铜的质量为:500吨×80%×80%=320吨.
故答为:(1)B;
(2)铁的硬度、密度比铝大;
(3)2Al+3CuO$\frac{\underline{\;高温\;}}{\;}$3Cu+Al2O3;在高温条件下,位于前面的金属能把位于后面的金属从它们的氧化物里置换出来;
(4)黑;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2 Fe+3CO2;可燃性,还原性,毒性;
(5)80%,320;
点评 本题主要考查了运用化学知识来解释生活中的问题,体现了化学与生活的紧密联系,难度不大.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
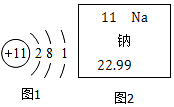 (1)某元素的原子结构示意图如图1所示,它属于金属(填“金属”或“非金属”)元素,该原子的核内有11个质子,在化学反应中容易失去电子成为阳离子.
(1)某元素的原子结构示意图如图1所示,它属于金属(填“金属”或“非金属”)元素,该原子的核内有11个质子,在化学反应中容易失去电子成为阳离子.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
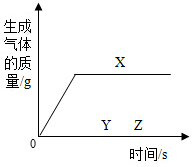 康康把等质量的X、Y、Z三种金属分别加入到同体积、同浓度的足量稀盐酸中,反应关系如图;Z加入YNO3的溶液中有Y生成.请判断:
康康把等质量的X、Y、Z三种金属分别加入到同体积、同浓度的足量稀盐酸中,反应关系如图;Z加入YNO3的溶液中有Y生成.请判断:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷又接触到氧气 | |
| B. | 燃烧时红磷转变成白磷,降低了着火点 | |
| C. | 红磷的温度还高于它的着火点 | |
| D. | 瓶内的氧气不能耗尽红磷 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在空气中燃烧产生白雾,放大量的热 | |
| B. | 氢气在空气中燃烧,发出淡蓝色火焰,放出大量的热 | |
| C. | 木炭在氧气中燃烧,发白光,放大量的热,生成二氧化碳 | |
| D. | 硫在氧气中燃烧,发出淡蓝色火焰,放出大量热,生成刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用带火星的木条可以检验氧气 | |
| B. | 用电解水的方法可以制取氧气 | |
| C. | 鱼类能在水中生活,证明氧气易溶于水 | |
| D. | 铁丝能在氧气中剧烈燃烧,火星四射,产生黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 小强在路边的围墙上看到一则化肥广告(如图):
小强在路边的围墙上看到一则化肥广告(如图):查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com