
����Ŀ�����о���ͼ�Ļ�ѧ����ʱ��ijС��ͬѧ��֤����ϡH2SO4��NaOH��Һ��Ϻ���Ȼ��Ϊ��ɫ��Һ����ȷʵ�����˻�ѧ��Ӧ����������һ�����ʵ�鷽������ơ�ʵʩ�����ۣ�
��1������һ���ⶨϡH2SO4��NaOH��Һ���ǰ���pH��20�棩�ⶨijNaOH��Һ��pH��pH____7��ѡ������������������������С����������һ������ϡH2SO4�����NaOH��Һ�У���Ͼ��Ⱥ�ⶨ��pH��pHС��7��
���ۣ�ϡH2SO4��NaOH��Һ�����˻�ѧ��Ӧ������__������
��2������������ʢ��NaOH��Һ���ձ����ȵμӷ�̪��Һ����μ�ϡ�������������۲쵽_____������
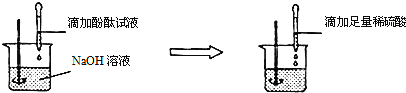
���ۣ�ϡH2SO4��NaOH��Һ�����˻�ѧ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ��_______��
��3�������������������˼���ϵ���ͬ����_______��
��4��Ϊ�˽�һ����ȡϡH2SO4��NaOH��Һȷʵ�����˻�ѧ��Ӧ��֤�ݣ������кͷ�Ӧ��_____��ѡ�������������������������������仯�����ķ�Ӧ������ͬ���µ�ϡH2SO4��NaOH��Һ����ʵ�飬����ʵ����������Ҫ�ⶨ��Һ�¶�_____�Σ�
��5��ʵ�����������ϡH2SO4��NaOH��Һ��ȫ��Ӧ������Һ15g���õ�Na2SO4����2.2g,�����Һ��______������͡��롰�����͡�������20��ʱNa2SO4���ܽ����22g)
���𰸡����� ϡH2SO4 ��̪�ȱ��ɫ�ٱ����ɫ H2SO4+2NaOH��Na2SO4+2H2O �ⶨ��Һ��Ӧǰ�������Ա仯��ȷ��������Һ��Ϻ��Ƿ�����ѧ��Ӧ ���� �� ������
��������
��1������������Һ�ʼ��ԣ���pH����7����������ԣ���pHС��7����һ������ϡH2SO4�����NaOH��Һ�У���Ͼ��Ⱥ�ⶨ��pH��pHС��7,˵��ϡH2SO4������
��2����ͼʾ���Կ�������ʵ��Ϊ����з�̪������������Һ�м���������ϡ���ᣬ�������ƺ����ᷴӦ���������ƺ�ˮ����ʵ�������Ϊ����̪�ȱ��ɫ�ٱ����ɫ����Ӧ�Ļ�ѧ����ʽΪ��H2SO4+2NaOH��Na2SO4+2H2O��
��3�������Dz���Һ��pH�����Ƿ�̪��ɫ�ı仯��������Һ������Ա仯�йأ��������������������˼���ϵ���ͬ���ǣ��ⶨ��Һ��Ӧǰ�������Ա仯��ȷ��������Һ��Ϻ��Ƿ�����ѧ��Ӧ��
��4���кͷ�ӦΪ���ȷ�Ӧ������ͨ���ⶨ��Ӧǰ����Һ���¶ȱ仯������ȷ������Ӧǰ����ʼ�¶ȣ���Ӧ�в��¶��Ƿ����ߣ���������������ٲ���Һ���¶��Ƿͣ������β�����Һ�¶ȣ�
��5��.ʵ�����������ϡH2SO4��NaOH��Һ��ȫ��Ӧ������Һ15g���õ�Na2SO4����2.2g����Һ��������������=![]() 100����
100����![]() 100�����ʸ���Һ�Dz�������Һ��
100�����ʸ���Һ�Dz�������Һ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ѧ��ȤС��ѧϰ���������ȡ���ռ������֪ʶ�����ܽᣬ����һ����룬�����������Ŀ���ݣ�

(1)д�������������ƣ�a________��
(2)����Eװ���ռ�������������Ӧ��________(����c������d��)��ͨ�롣
(3)װ��B��C����������ȡ������̼��װ��C�����װ��B�ڲ��������������____________���ø�װ��Ҳ������ȡ��������ȡ�����Ļ�ѧ����ʽΪ___________________������Fװ���ռ�CO2�����������ɵ�CO2��������������ˮ���ϼ�һ��ֲ���͵�Ŀ����__________________________��
��4��ʵ���ҳ��ü����������ƹ�����Ȼ�粒�����ȡ��������ͨ������°�����һ����ɫ���壬��������ˮ���ܶȱȿ���С��ʵ������ȡ����Ӧѡ�õķ������ռ�װ����________������ĸ��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס����������ֲ���ij��������������ͼ��ʾ������ͷ����ˮ���������׳�����a��ˮ������⺬�е���������OH����SO42����c��ˮ�������pH��7��ֻ����������NaCl�����ҳ��ŷŵ�b��ˮ�е����ʿ����ǣ�������
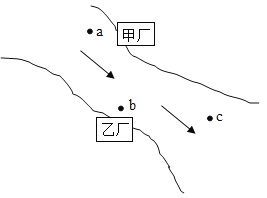
A. BaCl2��HClB. H2SO4��Ba��NO3��2
C. MgSO4��NaClD. H2SO4��MgCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС����������װ�ý����������ȡʵ��������ش��������⡣
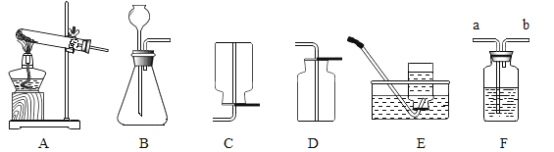
��1��д��װ��A��һ�ֲ�����������_____��
��2��A��E������ȡ����������ԭ����_____��дһ�㼴�ɣ���
��3��ʵ������ȡ������̼ѡ��ķ���װ����_____����ѡ����ĸ�������������̼�Ƿ��ռ����ķ�����_____��
��4�����ù���������Һ��ȡһƿ�����������Ҫ�õ�װ��F����װ��F��Ӧ�����������_____������Ӧ��_____��ͨ�루�a����b��������Fƿ��װ��ˮ���������ռ�ijЩ��������Ӧ��_____��ͨ�루�a����b����������ռ������������Ӧ��������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A-H��Ϊ���л�ѧ���������ʣ�����A��C�����Ԫ����ͬ�����壬��C�ܲ�������ЧӦ��BΪ����ɫ���dz��������Ҫ�ɷ֣�F���Ϻ�ɫ������H����ɫ������������ͼ��ʾ��ת����ϵ��ͼ�з�Ӧ����������ȥ������ش�
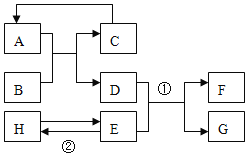
��1��д���������ʵĻ�ѧʽ��B______��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��______���÷�Ӧ�Ļ�����Ӧ������______����______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǹ�ҵ���Ʊ���������ʾ��ͼ�����в�ͬ��������������ͬ��ԭ�ӡ�����˵������ȷ���ǣ�������
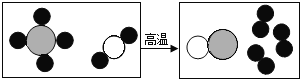
A. ͼ���ܱ�ʾ����ӵ�����![]() ��
��
B. �÷�Ӧ�й��漰���ֵ��ʺ����ֻ�����
C. ��Ӧǰ��ԭ�ӵ����ࡢ��Ŀ����
D. �÷�Ӧ�вμӷ�Ӧ�����ַ��ӵĸ�����Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��ͬѧ�α�����˿ȼ��ʵ���������Ȥ�����ǽ���������̽����
��̽��һ��ȡ���������ͬ�ļ���ƿ����������һ������ƿ�ռ�������Ȼ������ˮ������һ������ƿ���ռ������������Ƴ�����״����˿��ȼ��ֱ�������������ƿ�У��۲쵽��˿�ڿ����в���ȼ�գ����������п���ȼ�գ�Ϊʲô�����������������Ľ��ͣ�______����˿��������ȼ�յ������ǻ������䡢�ų��������ȡ�______������˿ȼ������ʱ������ɰֽ��ĥ��ԭ����______��
��̽��������ȤС��ͬѧ����˿ȼ���Ƿ�һ����Ҫ��������������Ȥ��������Ҫ����ˮ���ռ����������ֱ�Ϊ20%��40%��60%��80%���������ĸ�����ƿ�С���1����ȡһ��350mL�Ŀռ���ƿ����������Ϊ20%������ȡ200mLˮ�������У�Ȼ��ͨ�봿�����ų�150mLˮ���������ַ����ռ��������ĺ���Ϊ______������ȡ�ú���O2������______��
����˿��ȼ��ֱ���������ĸ�����ƿ�У�ʵ�鷢��ֻ������������20%�ļ���ƿ�е���˿����ȼ�գ��ɴ�ʵ��ó��Ľ�����______��
��̽��������ȤС��ͬѧ�ֲ����µIJ��룬��˿�ܹ�ȼ�գ��Ƿ�Ϳ�ȼ�ﱾ���йأ����Ƿֱ��û�ԭ�����ۡ����������ڿ����н���ʵ�飬ʵ����������������
��ԭ���� | �������� | |
��������mm�� | 1000 | 20-200 |
ʵ����������� | ֱ������ȼ�ŵľƾ��������ϣ��л��� | ֱ�Ӵ��ܷ�������������ʯ�����ϣ��л��� |
�ɴ�ʵ�����ܵó��Ľ����ǣ�______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ˮ��Ӧ������ˮú����������壩���䷴Ӧ����ʾ��ͼ������ʾ��
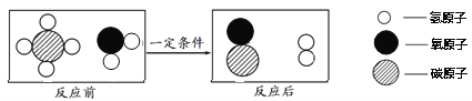
����������ʾ��ͼ�ó��Ľ����У���ȷ����
A����Ӧǰ���Ԫ�صĻ��ϼ۾�����
B��ˮú���ijɷ���һ����̼������
C���÷�Ӧ�к���Ԫ�صĻ�������3��
D���÷�Ӧ�Ļ�ѧ����ʽ�м����ˮ�ļ�����֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������м��Ҫ�ɷ������������������⣨Fe2O3������������������������ͼ��ʾ��
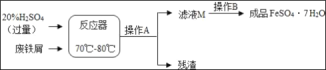
��1���ڷ�Ӧ���г�����Fe2O3+3H2SO4��Fe2��SO4��3+3H2O��Fe2��SO4��3+Fe�T3FeSO4��������Ӧ�⣬���ᷢ������һ����Ӧ����ѧ����ʽΪ��_____����Ӧ��Ҫ��ǿͨ�磬�Ͻ��̻���ԭ���ǣ�_____��
��2������Ʒ�����������±��գ���ת��ΪFe2O3��SO2��SO3��Ϊ�����SO3�IJ��ʣ�ijʵ��С�������ϵ��̽����ʵ���������£�
��� | ����ͨ����/Ls��1 | �¶�/�� | SO2����% | SO3����/% |
a | 0.02 | 850 | 45.4 | 54.6 |
b | 0.06 | 850 | 30.5 | 69.5 |
c | 0.10 | 810 | 11.1 | 88.9 |
d | 0.10 | 850 | 11.1 | 88.9 |
e | 0.10 | 890 | 11.2 | 88.8 |
����ʵ����Ҫ�о�����Щ���ض�SO3���ʵ�Ӱ��_____��
�������ϱ����ݣ����������в���ʵ��_____�����ţ�����ȡ�����������
�������ϱ����ݣ�������ͨ������SO3�IJ��ʵ�Ӱ�������_____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com