
分析 锌和稀硫酸反应生成硫酸锌和氢气,由参加反应的锌的质量,由反应的化学方程式列式计算出生成硫酸锌的质量、生成氢气的质量,进而计算出反应后所得硫酸锌溶液的溶质的质量分数.
解答 解:设生成硫酸锌的质量为x,生成氢气的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 161 2
6.5g x y
$\frac{65}{161}=\frac{6.5g}{x}$ x=16.1g
$\frac{65}{2}=\frac{6.5g}{y}$ y=0.2g
反应后所得硫酸锌溶液的溶质的质量分数是$\frac{16.1g}{6.5g+93.7g-0.2g}$×100%=16.1%.
答:反应后所得硫酸锌溶液的溶质的质量分数是16.1%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.


 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:选择题
| A. | 将二氧化碳通入紫色石蕊溶液中,溶液变红色 | |
| B. | 甲烷在空气中燃烧发出蓝色火焰,生成水和二氧化碳 | |
| C. | 硫在氧气中燃烧发出蓝紫色火焰 | |
| D. | 氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| 酸性 | 大→小 | ||||
| A. | H2SO4+2NaHCO3=2NaCl+2H2O+2CO2↑ | B. | 2HCl+CaS=CaCl2+H2S↑ | ||
| C. | CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO | D. | H2S+CuSO4=H2SO4+CuS↓ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ,请回答下列问题:
,请回答下列问题: ,W离子的离子符号为Na+;
,W离子的离子符号为Na+;查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 纸火锅(见图)在一些城市悄然兴起,这种纸火锅精巧漂亮,白色的底衬着火锅食料,干净、醒目;纸火锅在使用时无烟、无味;具有可以吸收汤里多余的杂质与油腻的特性,可维持汤底的清爽,让久煮的食物保留原本的鲜美.
纸火锅(见图)在一些城市悄然兴起,这种纸火锅精巧漂亮,白色的底衬着火锅食料,干净、醒目;纸火锅在使用时无烟、无味;具有可以吸收汤里多余的杂质与油腻的特性,可维持汤底的清爽,让久煮的食物保留原本的鲜美.查看答案和解析>>
科目:初中化学 来源: 题型:填空题


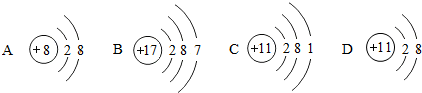
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com