
【题目】燃烧是生活中常见的现象。
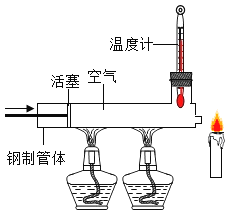
(1)已知石蜡的着火点约为190℃,蜡烛的火焰由气态石蜡燃烧形成。如图所示,在温度计读数为280℃以上时,快速推动活塞,观察到蜡烛立即熄灭。蜡烛熄灭的主要原因是什么?_____
(2)油库、面粉加工厂、加油站等场所都要严禁烟火,其原因是什么?_____
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】镁条在空气中久置表面会变黑。某小组同学设计并进行实验,探究镁条变黑的条件。
【查阅资料】常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
【猜想与假设】常温下,镁条变黑可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与镁条接触的物质,利用下图装置(镁条长度为3cm,试管容积为20mL),分别进行下列5个实验,并持续观察20天。
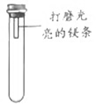
编号 | 主要实验操作 | 实验现象 |
1 | 先充满用NaOH浓溶液洗涤过的空气再加入2mL浓硫酸 | 镁条始终无明显变化 |
2 | 加入2mL NaOH浓溶液 | 镁条始终无明显变化 |
3 | 先加入2mL浓硫酸再通入约4mL CO2 | 镁条始终无明显变化 |
4 | 先加入4mL饱和Na2SO3溶液再充满CO2 | 镁条始终无明显变化 |
5 | 先加入2mL蒸馏水再通入约4mL CO2 | 镁条第3天开始变黑至第20天全部变黑 |
【解释与结论】
(1)实验1和2中,NaOH浓溶液的作用是 (用化学方程式表示)。
(2)实验1的目的是 。
(3)实验3中,试管内的气体主要含有CO2、 。
(4)得出“镁条变黑一定与CO2有关”结论,依据的两个实验是 (填编号)。
(5)由上述实验可推知,镁条变黑的条件是 。
【反思与评价】
(6)在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是 。
(7)欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需要的试剂是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乐平灯笼辣椒是景德镇十大特产之一,乐平灯笼辣椒种子曾带入神舟一号进行试验.有果面光滑,味微辣带甜,脆爽,果肉厚等特色.具有开胃消食、暖胃驱寒、促进血液循环、美容肌肤、止痛散热等特殊的保健功能.辣椒中维生素C含量居蔬菜之首位,维生素B、胡萝卜素以及钙、铁等矿物质含量亦较丰富.
(1)炒辣椒,闻到刺鼻的气味,说明粒子具有___的性质;
(2)辣椒中含有人体所需的营养素有___;
(3)钙是人体所需的常量元素,老年人人体缺钙通常会患___症状;
(4)辣椒中铁元素人体所需的微量元素,人体缺铁会患贫血.铁元素的部分信息如图,则下列说法中正确的是___(填字母).

A 铁原子中的核外电子数为26 B 铁离子中的核外电子数为26
C 铁原子核外电子层数为四 D 铁的相对原子质量为56
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验方法的设计中,不能达到实验目的是( )
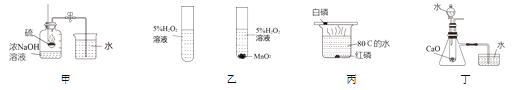
A.图甲测定空气中氧气的体积分数
B.图乙探究MnO2可加快H2O2的分解
C.图丙探究可燃物的燃烧是否需要与氧气接触
D.图丁验证CaO与水反应放热
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋蕴藏着丰富的自然资源.工业上可利用海水中的氯化镁来制取金属镁,其简化后的流程如图所示:
海水![]() 氢氧化镁
氢氧化镁![]() 氯化镁
氯化镁![]() 镁
镁
请回答下列问题:
(1)操作1的名称是__________.
(2)熟石灰与海水混合发生反应的化学方程式为__________.
(3)试剂X为__________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语图像往往能蕴含许多信息,从下列图示可以了解的信息中,其中不正确的( )

A.甲图是氟离子的结构示意图B.由乙图可知一个氩原子的质量为39.95
C.若“○”表示1个氮原子,则丙图表示1个氮分子D.丁图表示正一价的钠元素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你于他们一起进行以下探究.
(提出问题)溶液中的溶质是什么物质?
(作出猜想)
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质有Na2SO4和_____两种物质.
(3)丙同学认为溶液中的溶质有Na2SO4和NaOH两种物质.
(查阅资料)
①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和一种气体单质.
(实验验证)
实验操作 | 实验现象 | 实验结论 | |
乙同学实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管内的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
丙同学实验 | 取中和反应后的溶液少许于试管中,向试管内滴加几滴无色酚酞试液 | 无色溶液变成____色 | 猜想(3)成立 |
(总结反思)戊同学根据所学化学知识和乙、丙两同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,戊同学认为猜想(2)也不成立,他的理由是____.兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
(知识拓展)
(1)生活中能否用铝制品来盛放强碱性溶液?_____(选填“能”或“不能”)
(2)乙同学的实验中铝片与____溶液发生了反应,请写出铝与该溶液发生反应的化学方程式___.
(3)镁和铝在元素周期表中处于相邻位置,向盛有100g稀硫酸的烧杯中加入一定量的Mg粉,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示.
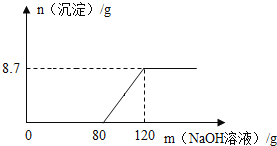
①计算该NaOH溶液溶质的质量分数____.(要求写出计算过程)
②计算该100g稀硫酸中所含溶质硫酸的质量为____g.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】往 64.5 克稀盐酸和氯化镁的混合溶液中,加入 20%的氢氧化钠溶液,所得溶液的 pH 变化与加入氢氧化钠溶液 的质量关系如图所示,试分析计算:
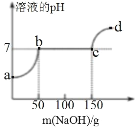
(1)a→b 段表示氢氧化钠与混合溶液中的_______________反应。
(2)反应到 c 点时,所得溶液的溶质质量分数是____________?(精确到 0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氨气可用于处理硝酸工厂排放的一氧化氮气体,该反应前后微粒种类如下图所示。下列说法正确的是

A.该反应不符合质量守恒定律
B.反应前后分子和原子的种类都不变
C.参加反应的X 和Y 的质量比为 30:17
D.反应生成的 Z 和W 的分子个数比为 5:6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com