
| A. | 净化水时,可用活性炭作杀菌剂 | |
| B. | 为使水中的悬浮杂质沉降,可在水中加入适量的明矾 | |
| C. | 用肥皂水可区分硬水和软水 | |
| D. | 生活中常用煮沸的方法降低水的硬度 |
分析 A、根据净水的知识进行分析,活性炭具有吸附性,能吸附色素和异味解答;
B、明矾溶于水形成的胶体能将不溶性固体小颗粒凝聚在其表面解答;
C、根据硬水中含有的可溶性钙镁化合物能与肥皂水混合产生浮渣,软水与肥皂水混合产生泡沫解答;
D、根据生活中常用煮沸的方法降低水的硬度解答.
解答 解:A、活性炭具有吸附性,能吸附色素和异味,不能起到杀菌的作用,故A错误;
B、明矾溶于水形成的胶体能将不溶性固体小颗粒凝聚在其表面,可以加速沉降,故B正确;
C、硬水中含有的可溶性钙镁化合物能与肥皂水混合产生浮渣,软水与肥皂水混合产生泡沫,可以使用肥皂水鉴别硬水和软水,故C正确;
D、生活中常用煮沸的方法降低水的硬度,故D正确;
故选A.
点评 本题考查了净水的知识,完成此题,可以依据已有的知识进行.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 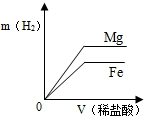 | B. | 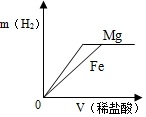 | C. | 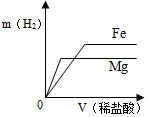 | D. | 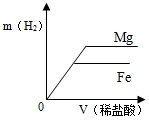 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加入催化剂能使化学反应的速率加快 | |
| B. | 不使用催化剂就不能发生化学反应 | |
| C. | 使用催化剂可以增加生成物的量 | |
| D. | 使用催化剂能改变化学反应的速率 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 有气泡放出,带火星的木条复燃. | Fe2O3质量仍为0.3g(或固体质量仍为0.3g) | 溶液中有气泡放出, 带火星木条复燃 | 猜想I成立; 猜想II、III不成立. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com