
| A. | 丁二酮是由C、H、O三种元素组成的 | B. | 丁二酮分子中含有氧分子 | ||
| C. | 丁二酮中各元素的质量比为2:3:1 | D. | 丁二酮中氢元素的质量分数为50% |
分析 A、根据化合物化学式的意义进行分析.
B、根据丁二酮的微观构成进行分析判断.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据化合物中元素的质量分数公式进行分析判断.
解答 解:A、丁二酮是由C、H、O三种元素组成的,故选项说法正确.
B、丁二酮是由丁二酮分子构成的,不含氧分子,故选项说法错误.
C、丁二酮中碳、氢、氧元素的质量比为(12×4):(1×6):(16×2)=24:3:16,故选项说法错误.
D、丁二酮中氢元素的质量分数为$\frac{1×6}{12×4+1×6+16×2}$×100%≈6.98%,故选项说法错误.
故选:A.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案科目:初中化学 来源: 题型:选择题
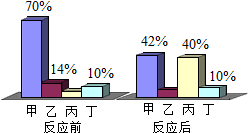 在密闭容器中有甲,乙丙丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如右图所示,下列说法正确的是( )
在密闭容器中有甲,乙丙丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如右图所示,下列说法正确的是( )| A. | 丙可能是单质 | |
| B. | 该反应属于化合反应 | |
| C. | 该反应中甲乙的相对分子质量之比14:3 | |
| D. | 丁一定是该反应的催化剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钙、熟石灰、Ca(OH)2 | B. | 氯化氢、盐酸、HCl | ||
| C. | 碳酸钙、熟石灰、CaCO3 | D. | 氧化钙、消石灰、CaO |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 为降低成本,用工业明胶制药胶囊 | |
| B. | 在乳制品中添加“皮革蛋白粉”,以提高蛋白质含量 | |
| C. | 目前我国多省份大力推广“加铁酱油”,以预防缺铁性贫血 | |
| D. | 将地沟油和泔水油回收用来炒菜,以达到变废为宝、节约资源的目的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
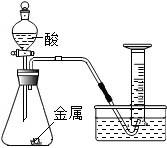 某化学兴趣小组探究“影响金属与酸反应速率的因素”,请你参与并回答问题:
某化学兴趣小组探究“影响金属与酸反应速率的因素”,请你参与并回答问题:| 实验编号 | 选用金属 (均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 0~1min | 1~2min | 2~3min | 3~4min | 4~5min | 前5min共收集气体 | |||
| Ⅰ | 锌片 | 10% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 47.6 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 用亚硝酸钠代替食盐来腌渍食品 | |
| B. | 大量出汗后,适量饮用含无机盐的饮料 | |
| C. | 羊毛、棉线都属于天然有机高分子材料,点燃后闻气味无法鉴别 | |
| D. | 每天摄入一定量的蔬菜、水果等含维生素较多的食物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
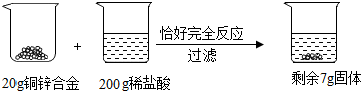
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
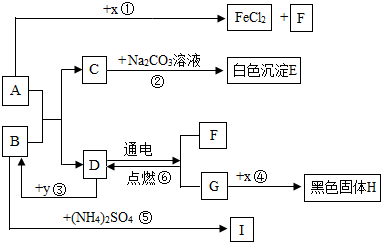
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com