
【题目】生活在密闭狭小的特殊环境(如潜艇、太空舱)里,O2会越来越少,CO2会越来越多,因此将CO2转化为O2,不仅有科学意义也有重要的实用价值。据科学文献报道,NiFe2O4在一定条件下既能促进CO2分解又可重复使用。NiFe2O4在此反应中是( )
A. 粘合剂B. 制冷剂C. 防腐剂D. 催化剂
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:初中化学 来源: 题型:
【题目】根据下列图示和相关叙述,回答下列问题。

(1)缺________(填元素名称)可能导致骨质疏松,易得佝偻病。
(2)图中硒的相对原子质量是_____。
(3)亚硒酸钠(Na2SeO3)可提高人体的免疫力,其中Se的化合价为__________。
(4)下列电动自行车的各组件中,属于合成材料的是_______。
a橡胶轮胎 b钢质车轮 c塑料灯罩
(5)香烟烟气中的____(填化学式)是一种极易与血液中的血红蛋白结合的有毒气体。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室里用64g浓度为12.5%的NaOH溶液和适量CO2气体反应制备纯Na2CO3(已知向NaOH溶液中通入过量CO2气体极易生成 NaHCO3,且无明显现象)。于是卢同学设计了如下实验方法:
①将64 g NaOH溶液等分成两份,分别是放在烧杯A、B中
②向A中通入过量CO2气体
③将A、B两烧杯中的液休混合后蒸干、灼烧。
(1)NaHCO3,属于__(填“酸”、“碱”或“盐”)。
(2)以上方法,步骤②中的方程式为:________:步骤③中的方程式为: NaOH+NaHCO3=Na2CO3+H2O。
(3)若直接向64 g NaOH溶液中通入过量CO2,再将溶液蒸干、灼烧,也能制得与卢同学等质量的纯Na2CO3。与卢同学的方法相比,该方法有何不足:_________。
(4) 卢同学制得了多少质量的纯Na2CO3_______?(请写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是学习和研究化学的重要工具,试根椐图示回答相应问题:
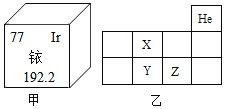
(1)2018年3月15日,央视曝光了知名珠宝品牌周大生黄金,在加工过程中掺有“杂质”――“铱”。
如图是铱元素在元素周期表中的信息,则铱元素属于_______(填“金属”或“非金属”)元素,铱原子的相对原子质量为_____。
(2)图乙是元素周期表中的一部分,X、Y、Z代表三种不同的元素,以下判断正确的是_____。
A 核外电子数 X=Y B 原子序数Z>Y C Y和Z处于同一周期
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数,探究过程如下:
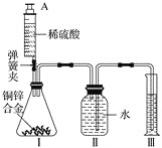
①连接实验装置并检查装置气密性。
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL(注:样品中的杂质不参加反应
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量为1.4g
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09gL-1。
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为___,实验过程中须加入稀硫酸至不再产生气体,目的是___。
(2)步骤③中称量剩余固体之前的正确操作是_______、洗涤、干燥。
(3)根据实验测定的数据,上述三位同学中________(填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数。
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差。以下因素可能造成偏差的有________(填标号)。
A 移出装置Ⅲ时,导管内留存了一部分水
B 实验测量前,没有排除装置Ⅰ中的空气
C 数据处理时,未排除加入稀硫酸所占的体积
【答案】(1)![]() ;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
【解析】
试题(1)由于铜排在了氢的后面,所以与酸不反应,反应物是锌和硫酸,生成物是硫酸锌和氢气,氢气后面标上上升符号;实验过程中须加入稀硫酸至不再产生气体,目的是使样品中的锌完全反应;(2)从铜和硫酸锌溶液的混合物中得到铜,先进行过滤,得到带有硫酸锌溶液的铜,再进行洗涤除去表面的硫酸锌,再进行干燥除去水即可;(3)根据加入稀硫酸的量进行计算需要知道稀硫酸的溶质质量分数,而题中没有告知;(4)由于锌与硫酸反应生成硫酸锌和氢气时,放出热量,如果没等冷却到室温,根据热涨冷缩的原理可知进入量筒中水偏多,所以误认为得到的氢气多,再就是数据处理时,未排除加入稀硫酸所占的体积,计算的结果就偏大;
考点:金属的化学性质;化学方程式;实验误差分析;
点评:熟记金属活动性顺序表,知道排在氢之前的金属和稀盐酸或者硫酸反应生成氢气,而排中氢之后的金属和稀盐酸或者稀硫酸不生成氢气;化学反应中物质的质量比都是纯净物之间的质量比,而溶液中溶质的质量=溶液质量×溶质质量分数;本题容易出错的地方是对实验结果的评价,要知道锌与硫酸反应放出热量,会造成相应的误差,必须冷却到室温才能进行观察和计算。
【题型】实验题
【结束】
30
【题目】用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某金属冶炼厂的管道烟泥中含有Cu、Zn及炭黑,现欲回收铜和锌,主要流程如图所示:
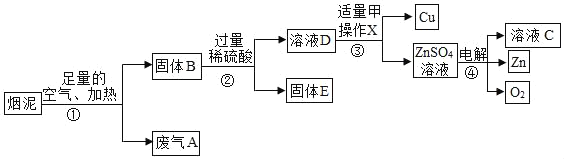
(1)步骤①产生的废气A中,一定含有的气体是_____。
(2)溶液D中一定含有的溶质是_____。
(3)步骤③中发生反应的化学方程式是_____(任写一个)。操作X的名称是_____;其所需玻璃仪器除漏斗、玻璃棒外,还有_____。
(4)步骤④中参加反应的物质为ZnSO4和_____(填化学式)。
(5)有人认为若步骤①中空气不足量,会导致锌的回收率降低,你认为是否正确?_____(填“正确”或“不正确”),理由是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化工生产中的废弃物再利用,可以有效节约资源、保护环境,下图是某化工厂利用废硫酸制备K2SO4的工艺流程图:
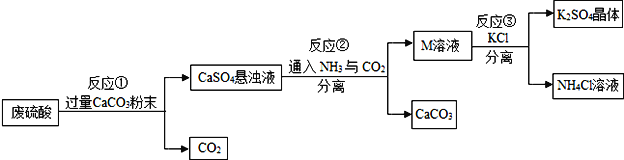
(1)生产上将CaCO3研成粉末的目的是______;
(2)写出反应![]() 的化学方程式______;
的化学方程式______;
(3)反应②充分反应后物质分离的方法是______;
(4)上述流程中,M溶液中溶质的主要成分是______(填写化学式);
(5)分析下表所示数据,则反应③在常温下可实现的原因是______;
物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(6)洗涤反应③所得晶体最适宜的试剂是______(填序号);
AH2O B饱和K2SO4溶液 C 不饱和K2SO4溶液 D三者均可
(7)检验K2SO4晶体是否洗涤干净的方法是________________________________________。
(8)取50t质量分数为9.8%废硫酸用于该工艺制备K2SO4,理论可得到K2SO4质量为____t。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组利用稀盐酸和澄清石灰水展开“酸碱中和反应”的实验探究活动。请你参与他们的实验活动,并回答相关问题
(提出问题Ⅰ)稀盐酸和澄清石灰水能否发生反应?
(实验1)小明取一定量的稀盐酸,测得其pH=2,然后向其中加入一定量的澄清石灰水后,测得混合溶液的pH=3,于是得出“稀盐酸和澄清石灰水发生了中和反应”的结论。
测定溶液pH的方法是:将pH试纸放在玻璃片上,___,将试纸显示的颜色与标准比色卡比较。
小刚认为,小明的实验方案不能证明二者发生了中和反应,理由是___。
(实验2)小刚取稀盐酸于试管中,加入一定量的澄清石灰水,得到溶液X,再加入适量铁粉,观察到___,证明稀盐酸和澄清石灰水发生了反应。
稀盐酸和澄清石灰水反应的化学方程式为___。
(提出问题Ⅱ)溶液X中溶质的成分是什么?
猜想一:只有CaCl2;猜想二:CaCl2和Ca(OH)2;猜想三:CaCl2和HCl
小组同学为验证猜想二,进行了如下实验(查阅资料显示CaCl2溶液显中性)
实验操作 | 实验现象 | 实验结论 | |
实验3 | 取适量溶液X于试管中,滴加紫色石蕊溶液 | ___ | 猜想二成立 |
实验4 | 取适量溶液X于试管中,滴加Na2CO3溶液 | 产生白色沉淀 | 猜想二成立 |
小明认为实验4中产生白色沉淀,并不能证明猜想二成立,理由是____。
请你另选一种试剂,设计合理的方案,当观察到与实验4相同的现象时,证明猜想二成立。你的实验原理是___(用化学方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com