
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:初中化学 来源: 题型:阅读理解
| 指标 | 检测项目及单位 | 限值 |
| 微生物指标 | 总大肠杆菌群(MPN/100ml) | 不得检出 |
| 感官性状指标 | 臭和味 | 无异嗅、无异味 |
| 肉眼可见物 | 无 | |
| 一般化学指标 | pH | 不小于6.5且不大于8.5 |
| 总硬度(以CaCO3计)(mg/l) | 450 | |
| 溶解性总固体( mg/l) | 1000 |
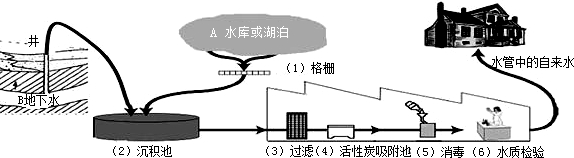
查看答案和解析>>
科目:初中化学 来源: 题型:
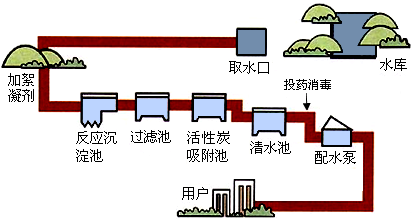
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
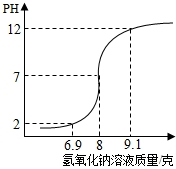 (2013?温州)小明在老师的指导下测一瓶稀盐酸的溶质质量分数,具体步骤如下:
(2013?温州)小明在老师的指导下测一瓶稀盐酸的溶质质量分数,具体步骤如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com