
【题目】(1)历史上,道尔顿认为,原子是一个个简单的、不可分割的实心球体。现在你认为该观点___(选填“正确”或“错误”)。
(2)元素周期律是学习和研究化学的重要工具。下表是元素周期表的部分信息:
1H 氢 | 2He 氦 | |||||||
3Li 锂 | 4Be 铍 | 5B 硼 | 6C 碳 | 7N 氮 | 8O 氧 | 9F 氟 | 10Ne 氖 | |
llNa 钠 | 12Mg 镁 | 13A1 铝 | 14Si 硅 | 15P 磷 | 16S 硫 | 17C1 氯 | 18Ar 氩 | |
19K 钾 | 20Ca 钙 | …… | ||||||
认真分析信息,回答:
 表示的是(填名称)__________;
表示的是(填名称)__________;
(3)上表中每一周期元素原子序数的变化规律是____________________________。
(4)上表中硫元素的每个原子需要得到___个电子形成相对稳定结构的离子,该离子与Na+形成化合物的化学式为___。
(5)亚氯酸钠(NaClO2)是一种重要的消毒剂,其中氯元素的化合价为___。
【答案】 错误 Cl- 从左到右原子序数依次增大 2 Na2S +3
【解析】(1)历史上,道尔顿认为,原子是一个个简单的、不可分割的实心球体。现在认为该观点是错误的。(2)元素周期律是学习和研究化学的重要工具。 表示的是Cl-,核内17个质子,核外18个电子。 (3)每一周期元素原子序数的变化规律是从左到右原子序数依次增大。(4) 硫元素的每个原子需要得到2个电子形成相对稳定结构的离子,根据正负总价代数和为零原则,该离子与Na+形成化合物的化学式为Na2S。(5)亚氯酸钠(NaClO2)是一种重要的消毒剂,其中氯元素的化合价为∶﹙+1﹚+x+﹙-2﹚×2=0,x=+3 .
表示的是Cl-,核内17个质子,核外18个电子。 (3)每一周期元素原子序数的变化规律是从左到右原子序数依次增大。(4) 硫元素的每个原子需要得到2个电子形成相对稳定结构的离子,根据正负总价代数和为零原则,该离子与Na+形成化合物的化学式为Na2S。(5)亚氯酸钠(NaClO2)是一种重要的消毒剂,其中氯元素的化合价为∶﹙+1﹚+x+﹙-2﹚×2=0,x=+3 .
点睛∶原子并不是一个个简单的、不可分割的实心球体,具有复杂的内部结构。原子可以通过得失电子变为离子,化学式的书写应符合正负总价代数和为零原则。


科目:初中化学 来源: 题型:
【题目】对课本的实验改进是创新精神和能力的体现;宏观实验、微观探析是化学学习的重要方式和途径。
【问题情景】在课外活动中,小萍按照课本实验(见图1)探究分子的运动时,闻到了刺激性的氨味,于是,小萍在老师的指导下,设计了如图2的实验装置,进行同样的实验,可以迅速观察到明显现象,得到了和课本实验同样的结论。
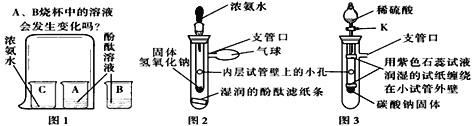
【实验探究与结论】小萍用图2装置进行实验。
(1)滴入少量浓氨水后,湿润的酚酞滤纸条发生的变化是______________;
从分子运动的角度分析,此现象可说明的结论是_________________________。
(2)用初中的化学知识分析,固体氢氧化钠的作用是_____________________________。(提示:氢氧化钠固体能溶于水且放出大量热量)
(3)和课本实验比较,小萍改进后的装置的优点是___________________(只需写一点)。
【思维拓展】小蕊受小萍实验的启发,将图2装置进一步改装成图3装置,用于验证二氧化碳的性质。
(4)小蕊查阅资料得知:稀硫酸中含有硫酸(化学式H2SO4),没有挥发性,可与碳酸钠反应生成二氧化碳、硫酸钠和水,写出上述反应的符号表达式_____________________。
(5)打开活塞K滴入稀硫酸后,两条用紫色石蕊试液润湿的试纸发生的相同变化是________________,不同变化是_____________________,小蕊从课本实验中知道,二氧化碳和水本身都不能使石蕊变色,因而她认为以上两个变化验证的二氧化碳的性质分别是___________________、______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解成丙;它们之间有如右图所示的转化关系(部分物质和反应条件已经略去)。
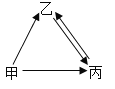
(1)甲的化学式为_________________;
(2)乙转化成丙的化学方程式为________________________________;
(3)甲转化成丙的反应基本类型为__________________________________
(4)甲、乙、丙三种物质中属于单质的是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】只有正确认识了物质,才能合理改造和应用物质.请你运用归纳/演绎、实验、比较/对比等科学方法认识氯化钠.
(1)用归纳演绎法认识氯化钠的性质
已知下列反应:HCl+AgNO3=AgCl+HNO3 MgCl2+2AgNO3=2AgCl↓+Mg(NO3)2
①上述反应属于四种基本反应类型中的______,运用(填“归纳”或“演绎”)______法得到这组反应发生的原因是______.
②由①中得到的规律可以推测“氯化钠溶液也能跟硝酸银溶液反应”,运用的是(填“归纳或“演绎”)______法.
(2)用实验法认识氯化钠的性质
①要验证(1)②中“氯化钠溶液也能跟硝酸银溶液反应”的推断,需要进行实验,实验方法是______,反应的化学方程式是______.
②有实验法认识氯化钠溶液的酸碱性,其实验方法是______.
比较是为了找出事物的相同点,对比是为了找出事物的不同点.
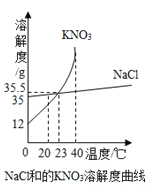
图为氯化钠和硝酸钾溶解度曲线,通过比较/对比可以发现二者的相同点有(选字母编号,下同)______,不同点有______.
A、易溶物质 B、溶解度随温度变化的方向 C、溶解度受温度影响的程度
D、20℃时的饱和溶液溶质质量分数 E、23℃时的溶解度
F、40℃100g饱和溶液降温到20℃析出晶体的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气中氧气含量测定的再认识.
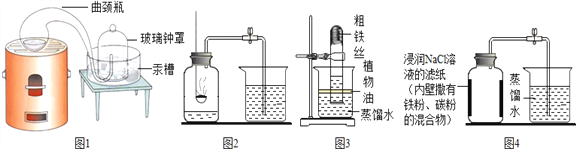
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有 ____________.
A.实验过程中没有污染
B.在汞槽中起到液封作用
C.生成的化合物加热分解又能得到汞和氧气
D.能将密闭装置内空气中的氧气集合耗尽
【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的文字表达式________.兴趣小组用该方法测出的氧气含量常常远低于21%.
【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行猜想】(1)装置漏气;(2)_________装置内氧气有剩余;…
【实验探究1】小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图3)通过7天测得的数据计算空气中氧气的含量为19.13%.
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定结果更准确的原因:___________________.
【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4),8分钟后测得的数据如表:
实验前的体积 | 实验后的体积 | |
集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
131mL | 90.0mL | 63.6mL |
请计算出空气中氧气含量________(计算结果保留一位小数)
【结论与反思】通过上述实验探究,选择________(填物质名称)进行实验,可较为快速地完成实验并减小实验误差.
【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3],若将图3装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由。 ________(填“能”或“不能”),理由____________。(提示:铜与空气中氧气、水、二氧化碳反应锈蚀时,当参加反应的氧气和二氧化碳的体积相等时,反应才能恰好完成。)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验是进行科学探究的重要方式。某同学设计如下图所示实验,探究二氧化碳的有关性质。
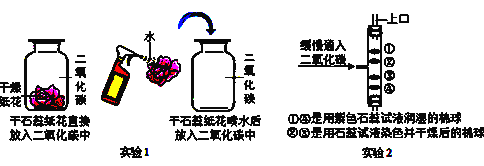
请填空:
(1)实验1中干石蕊纸花喷水后放入二氧化碳中,观察到的现象是_________,该反应的化学方程式是_______________________________。
(2)实验2是在实验1的基础上设计的创新改进实验,将二氧化碳缓慢通入竖直放置的玻璃管中,能观察到第________(填序号)号棉球先变色,通过此现象可获得关于二氧化碳的另外一条性质是____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组同学为了验证质量守恒定律,做了镁条在空气中燃烧的实验。
(1)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量。有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是:________________________
(2)细心的同学发现白色固体产物中还有少量黄色固体。经查阅资料并实验论证后同学们知道了镁条在空气中点燃时,除了能与氧气反应还能与氮气剧烈反应化合生成黄色的氮化镁(Mg3N2)固体。
① 氮化镁中氮元素的化合价是_________________;
② 空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是:___________________________________________;
③ 请写出镁与氮气反应的化学方程式:________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com