
| 试验编号 | 方案1 | 方案2 | 方案3 |
| 实验操作(分别取少量实验后的溶液于试管中) | 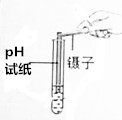 | 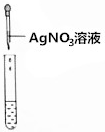 | 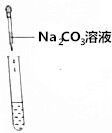 |
| 实验现象 | 对照标准比色卡:pH<7 | 产生白色沉淀 | 有气泡产生 |
| 实验结论 | 猜想二成立 | ||
分析 根据已有的知识进行分析解答,实验室使用碳酸钙和稀盐酸反应制取二氧化碳气体;对反应后溶液中的溶质成分猜测,就是检测是否含有盐酸,根据酸的性质进行分析解答即可.
解答 解:【提出猜想】碳酸钙和稀盐酸反应生成绿化钙、水和二氧化碳,故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;
【实验探究】若是含有盐酸,则加入碳酸钠会产生气体,故填:有气泡产生;
【评价反思】(1)①测定溶液的pH,不能将pH试纸直接浸入待测液中,故填:将pH试纸直接浸入了待测液中;
②方案二中,加入硝酸银溶液,即使没有盐酸,硝酸银也会与氯化钙溶液反应产生白色沉淀,故加入硝酸银不能确定是否含有盐酸,故填:没有盐酸,硝酸银也会与氯化钙溶液反应产生白色沉淀,故加入硝酸银不能确定是否含有盐酸;
(2)剩余的固体可能是碳酸钙中不参加反应的杂质,故不能确定盐酸没有剩余,故填:剩余的固体可能是石灰石中不参加反应的杂质.
点评 本题考查的是物质的成分的确定,完成此题,可以依据已有的物质的性质以及物质间反应的实验现象进行.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 锌、铁等金属能置换出酸中的氢气 | |
| B. | 盐酸能除去铁锈,将生锈的铁钉长时间浸泡在盐酸中,除锈效果会更好 | |
| C. | 铁丝与硫酸铜溶液反应后固体质量会增加 | |
| D. | 铝比铁的抗腐蚀能力强的原因是因为铁的化学性质比铝活泼 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH 氢氧化钠 烧碱 | B. | CaO 氢氧化钙 生石灰 | ||
| C. | Na2CO3 碳酸钠 纯碱 | D. | NaCl 氯化钠 食盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验内容 | 冷的铜线圈 | 热的铜线圈罩住火焰 | |
| 置于火焰中部 | 完全罩住火焰 | ||
| 实验现象 | 上层火焰中部 下层火焰继续燃烧 | 熄灭 | 不熄灭照常燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
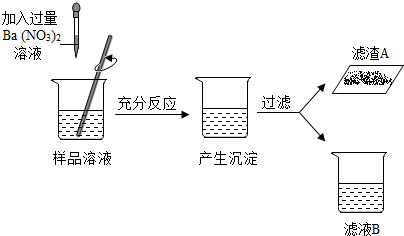
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com