
[ ]
A.45.8g B.45.8% C.22.9g D.31.4% E.31.4g
科目:初中化学 来源: 题型:阅读理解
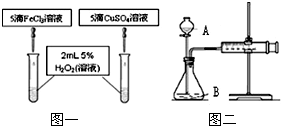
 在我校实验室实施的扬州市2011年中考化学实验操作考查刚刚落下帷幕.实验考查中H2O2分解制氧气为何不采用MnO2作催化剂?同学们为之展开了探究.
在我校实验室实施的扬州市2011年中考化学实验操作考查刚刚落下帷幕.实验考查中H2O2分解制氧气为何不采用MnO2作催化剂?同学们为之展开了探究.| 催化剂及用量 | O2 平均产量 | 制氧所需时间 | 成本 | 反应情况 |
| MnO21.0g | 919mL | 10′03″ | 0.11元 | 分解先快后慢 |
| 10%FeCl3溶液5滴 | 985mL | 4′50″ | 0.02元 | 均匀产生O2 |
| 15%CuSO4溶液5滴 | 955mL | 4′57″ | 0.03元 | 均匀产生O2 |
| ||
| ||
| 浓度 时间(min) 条件 |
30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
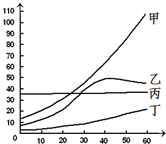 结合表列出几种物质在不同温度时的溶解度回答以下问题.
结合表列出几种物质在不同温度时的溶解度回答以下问题.| 温度/℃ | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | |
| 溶解度/g | 高锰酸钾 | 2.8 | 4.3 | 6.4 | 9.0 | 12.6 | 18.0 | 22.1 |
| 碳酸钠 | 7.0 | 12.5 | 21.5 | 39.5 | 49.0 | 48.0 | 45.0 | |
| 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | |
| 硝酸钾 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
查看答案和解析>>
科目:初中化学 来源:2013-2014学年上海市普陀区中考期末(一模)考试化学试卷(解析版) 题型:探究题
测定溶解度有多种方法,下列是测定30℃时硫酸铜溶解度的实验方法。经查找资料,30℃时硫酸铜的溶解度为25g/100gH2O。
一、配置30℃时的硫酸铜饱和溶液:
(1)配置的步骤如图:

取用100mL水,图中称量得到22.2g硫酸铜用于实验,是否合理,请说出理由 ;并在30℃的水浴中加热硫酸铜溶液一段时间,保证硫酸铜完全溶解,得到饱和溶液。
二、测量一定质量饱和硫酸铜溶液中硫酸铜的质量:
(2)在已配得的30℃时饱和溶液中,迅速取出饱和溶液50g,采用蒸发的方法求得硫酸铜的质量。从饱和溶液中析出蓝色晶体的化学式为(10) ,得到晶体后还要继续加热,直至固体颜色变为(11) 色为止。此操作过程中,用到的仪器除铁架台、酒精灯外,还需(12) 。
(3)最后称量得到固体质量为9.8g,经计算得到此时硫酸铜的溶解度为(13) g/100gH2O(精确到0.1g)。实验反思:实验数值比资料中的数据偏小,可能的原因是(14) (写出一条即可);
(4)测量50g饱和硫酸铜溶液中硫酸铜的质量,还可以使用重量法。
实验原理:CuSO4+BaCl2 →CuCl2+BaSO4↓
该实验方法中一定还要用到的实验操作是(15) (填写操作名称)。若最终得到硫酸钡14.5g,计算溶液中硫酸铜的质量为多少克?(提示:硫酸铜式量为160,硫酸钡式量为233。写出计算过程,精确到0.1g)
查看答案和解析>>
科目:初中化学 来源: 题型:
测定溶解度有多种方法,下列是测定30℃时硫酸铜溶解度的实验方法。经查找资料,30℃时硫酸铜的溶解度为25g/100gH2O。
 一、配置30℃时的硫酸铜饱和溶液:
一、配置30℃时的硫酸铜饱和溶液:
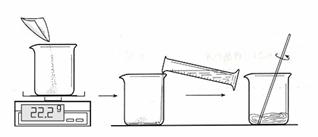
①配置的步骤如图:
取用100mL水,图中称量得到22.2g硫酸铜用于实验,是否合理,请说出理由(9) ;并在30℃的水浴中加热硫酸铜溶液一段时间,保证硫酸铜完全溶解,得到饱和溶液。
二、测量一定质量饱和硫酸铜溶液中硫酸铜的质量:
②在已配得的30℃时饱和溶液中,迅速取出饱和溶液50g,采用蒸发的方法求得硫酸铜的质量。从饱和溶液中析出蓝色晶体的化学式为(10) ,得到晶体后还要继续加热,直至固体颜色变为(11) 色为止。此操作过 程中,用到的仪器除铁架台、酒精灯外,还需(12) 。
程中,用到的仪器除铁架台、酒精灯外,还需(12) 。
③最后称量得到固体质量为9.8g,经计算得到此时硫酸铜的溶解度为(13) g/100gH2O(精确到0.1g)。实验反思:实验数值比资料中的数据偏小,可能的原因是(14)
(写出一条即可);
④测量50g饱和硫酸铜溶液中硫酸铜的质量,还可以使用重量法。
实验原理:CuSO4+BaCl2 →CuCl2+BaSO4↓
该实验 方法中一定还要用到的实验操作是(15) (填写操作名称)。若最终得到硫酸钡14.5g,计算溶液中硫酸铜的质量为多少克?(提示:硫酸铜式量为160,硫酸钡式量为233。写出计算过程,精确到0.1g)
方法中一定还要用到的实验操作是(15) (填写操作名称)。若最终得到硫酸钡14.5g,计算溶液中硫酸铜的质量为多少克?(提示:硫酸铜式量为160,硫酸钡式量为233。写出计算过程,精确到0.1g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com