
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| ①将NaOH溶液加热煮沸 | ①除去溶液中的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想不正确(填“正确”或不正确”) |
| ②向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | ②隔绝氧气 |
分析 【猜想与假设】将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了.除了题目中的猜想,还可考虑酸与碱发生中和反应;
【设计实验】
(1)甲同学认为“可能是酚酞与O2发生了反应”,隔绝氧气,设计了实验;
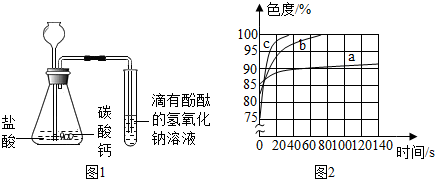
(2)乙同学认为“可能是NaOH溶液与空气中的CO2发生了反应”,设计如图1装置进行实验,则正确写出CO2与NaOH溶液反应的化学方程式,考虑二氧化碳中可能混有氯化氢气体;
(3)认真分析(3)题图可以得出:氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越大,起始颜色越深.从图中看5%的NaOH溶液滴加2滴酚酞试液后140s内色度从85升高至92,那么从92升高至100,所需时间要大于140s.
解答 解:【猜想与假设】将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了.除了题目中的猜想,还可考虑酸与碱发生中和反应;滴入酚酞溶液的多少、滴入酚酞溶液的浓度大小以及氢氧化钠溶液的浓度、氢氧化钠溶液中含有的杂质等;
【设计实验】
(1)甲同学认为“可能是酚酞与O2发生了反应”,隔绝氧气,设计了如下实验:
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| ①将NaOH溶液加热煮沸 | ①除去溶液中的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想 不正确(填“正确”或不正确”) |
| ②向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | ②隔绝氧气 |
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| ①将NaOH溶液加热煮沸 | ①除去溶液中的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想 正确(填“正确”或不正确”) |
| ②向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | ②隔绝氧气 |
点评 本题考查了如何探究物质的性质和变化规律,掌握反应现象与本质的联系、学会猜想和事实验证的方法是解题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
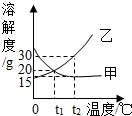 (1)如图是甲、乙两物质的溶解度曲线,试回答:
(1)如图是甲、乙两物质的溶解度曲线,试回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用紫色石蕊试液可以区分氢氧化钠溶液和澄清石灰水 | |
| B. | 用观察颜色的方法可鉴别磷矿粉和硫酸铵 | |
| C. | 用适量BaCl2溶液可除去KNO3溶液中混有的K2SO4 | |
| D. | 配制一定溶质质量分数的稀硫酸时,应将水倒入浓硫酸中稀释 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 几天后,三份固体的质量为:A=B=C | |
| B. | 为控制正好反应,A能用酚酞试液指示,B、C可滴加稀硫酸直到正好不冒气泡 | |
| C. | 正好反应时,消耗稀硫酸的质量由大到小的顺序为:A>B>C | |
| D. | 正好反应时,生成硫酸钠的质量都相等,均为35.5g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com