
| A. | 98千克 | B. | 100千克 | C. | 102千克 | D. | 104千克 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:计算题
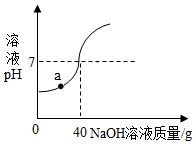 中和反应在工农业生产中应用广泛.现将溶质质量分数为10%的氢氧化钠溶液滴加到60g稀硫酸中,测得溶液pH与加入的氢氧化钠溶液的质量关系如图所示.
中和反应在工农业生产中应用广泛.现将溶质质量分数为10%的氢氧化钠溶液滴加到60g稀硫酸中,测得溶液pH与加入的氢氧化钠溶液的质量关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验装置 | 实验步骤及操作 | 实验现象 |
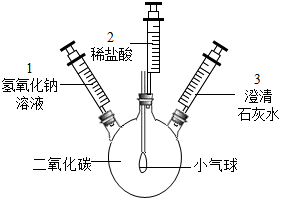 | ①将注射器1中的溶液推入充有CO2的瓶中 | 气球鼓起 |
| ②… | 无明显现象 | |
| ③将注射器2中的溶液推入瓶中 | 溶液中有气泡产生气球变瘪 | |
| ④向外拉注射器3 | 澄清石灰水变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
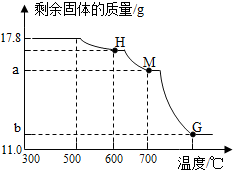
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分.
某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分.| 实验 | 现象 | 结论 | |
| 实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | 说明水垢中一定没有 氢氧化钙 |
| 实验二 | 按如图所示方案进行实验 | 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 水垢中一定含有 碳酸钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 鉴别的物质 | 鉴别的方法 |
| A | 纯水和矿泉水 | 观察是否澄清 |
| B | 硬水和软水 | 加肥皂水,振荡,观察泡沫的多少 |
| C | 水和过氧化氢溶液 | 加二氧化锰,观察是否有气泡 |
| D | 二氧化碳和氮气 | 加澄清石灰水,振荡,观察是否变浑浊 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com