
| A. | HNO3、KOH、CuSO4 | B. | Ca(OH)2、HCl、NaCl | ||
| C. | H2SO4、Na2CO3、Ba(OH)2 | D. | KNO3、NaOH、HCl |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 水分解成氢气和氧气的过程是物理变化 | |
| B. | 和负极相通的玻璃管内生成的气体是氧气 | |
| C. | 和正极相通的玻璃管内生成的气体是氢气 | |
| D. | 这个实验说明了水是由氢元素和氧元素组成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加入氯化钡溶液,产生白色沉淀 | |
| B. | 加入石灰水产生无色气体 | |
| C. | 加入稀盐酸产生了能使石灰水变浑浊的气体 | |
| D. | 放入水中,不溶解的碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可能存在Na2SO4 | B. | 可能存在NaOH | ||
| C. | 肯定不存在BaCl2 | D. | 肯定存在Na2CO3和Na2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
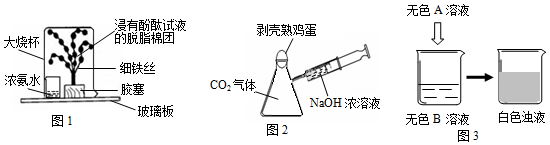
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
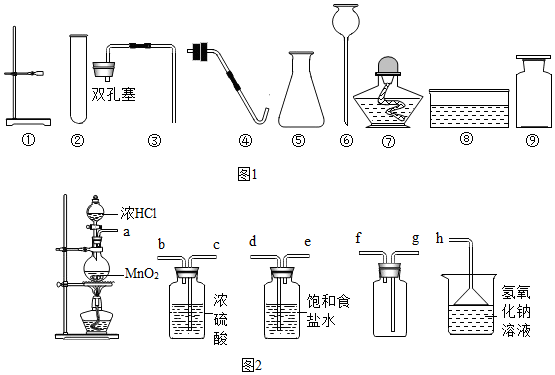
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 炎热的夏季,很多同学饮用一种补充人体盐分的饮品--盐汽水,你认为盐汽水的成分和普通汽水最大的不同是增加了( )
炎热的夏季,很多同学饮用一种补充人体盐分的饮品--盐汽水,你认为盐汽水的成分和普通汽水最大的不同是增加了( )| A. | 盐酸 | B. | 氯化钠 | C. | 二氧化碳 | D. | 碳酸钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
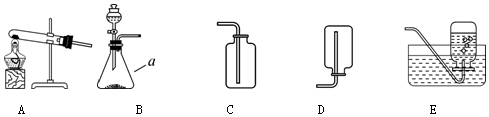
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com