


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:初中化学 来源: 题型:
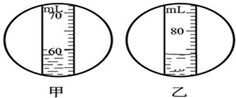 15.4gNaCl完全溶解在如图甲所示的水中,将完全溶解后所得溶液全部倒入原量筒中,液面位置如图乙,则所得NaCl溶液的密度为
15.4gNaCl完全溶解在如图甲所示的水中,将完全溶解后所得溶液全部倒入原量筒中,液面位置如图乙,则所得NaCl溶液的密度为查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
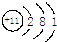 ,该原子在化学反应中易
,该原子在化学反应中易查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com