
| A. | 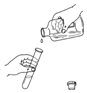 倾倒液体 | B. | 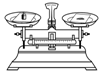 称量固体 | ||
| C. | 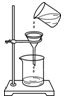 过滤 | D. | 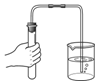 检查装置的气密性 |
分析 A、取用液体时:注意瓶口、标签的位置,瓶塞的放置等;
B、根据托盘天平的使用方法:左托盘放称量物,右托盘放砝码,进行分析解答;
C、过滤液体时,要注意“一贴、二低、三靠”的原则;
D、根据检查装置气密性的方法进行分析判断.
解答 解:A、取用液体时:①试剂瓶瓶口要紧挨试管口,防止液体流出;②标签向着手心,防止液体流出腐蚀标签;③瓶塞倒放桌面上,防止污染瓶塞,从而污染药品,所以图中操作错误;
B、根据托盘天平称物时:左托盘放称量物,右托盘放砝码,因此称量固体操作错误;
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流、漏斗下端没有紧靠在烧杯内壁上,图中所示操作错误.
D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确;
故选D
点评 了解具备基本的化学实验技能是学习化学和进行化学探究活动的基础和保证;掌握化学实验的基本技能,才能安全、准确地进行化学实验.


科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
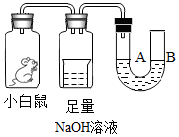 根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )| A. | A处上升,B处下降 | B. | A、B两处都下降 | C. | A处下降,B处上升 | D. | A、B两处都不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 据新闻报道某城镇边的一条河中惊现红色河水,被称为“红色多瑙河”,原来是某印染厂将积存的印染废水趁大雨倒入河水中,造成水体污染.
据新闻报道某城镇边的一条河中惊现红色河水,被称为“红色多瑙河”,原来是某印染厂将积存的印染废水趁大雨倒入河水中,造成水体污染.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 可以降低煤的着火点 | |
| B. | 可以减少有害气体的产生 | |
| C. | 可以使煤成为绿色燃料 | |
| D. | 能增加与氧气的接触面积,能使煤充分燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
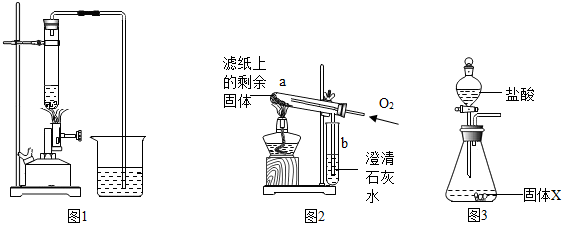
| 步骤 | 操作 | 主要现象 | 结论 |
| I | 取部分冷却后的固体X倒在滤纸上,用磁铁充分吸引. | 部分固体被吸引到磁铁上 | 可能有Fe或Fe3O4 |
| II | 取滤纸上的剩余固体少量,放入图2所示的试管a中,通入氧气,用酒精灯加热. | 固体剧烈燃烧,b中溶液变浑浊 | 一定有C. |
| III | 另取滤纸上的剩余固体少量,放入试管中,加入足量的稀盐酸. | 无明显现象 | 一定没有FeO和Fe2O3 . |
| IV | 取步骤I磁铁上的固体少量,放入试管中,逐滴加入稀盐酸. | 产生产生气泡. | 一定有Fe |
| V | 在步骤IV所得溶液中逐滴加入KSCN溶液. | 溶液不变红色 | 一定没有Fe3O4 |
| 步骤 | 操作 | 数据 |
| I | 重新取部分冷却至室温的固体X,称量其质量为m1. | m1=17.9g |
| II | 将称量好的固体X全部放入图3所示的锥形瓶中,称量整套装置及药品的质量为m2;打开分液漏斗旋塞,放入足量稀盐酸后关闭旋塞,待没有气泡产生并恢复至室温,再次称量整套装置及药品的质量为m3. | m2=317.9g m3=317.3g |
| III | 将锥形瓶中剩余的固体过滤、洗涤并干燥,称量其质量为m4. | m4=1.1g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验用剩的药品,不要抛弃,不要带出实验室,应放回原试剂瓶 | |
| B. | 加热后的试管立即用冷水冲洗 | |
| C. | 倾倒试液时,为了能看到标签,标签背对着手心 | |
| D. | 给试管里的液体加热时,试管口不能朝着任何人 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com