
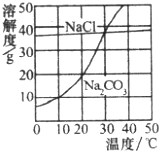
 如图所示为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”.请你解释“夏天晒盐,冬天捞碱”的原因.
如图所示为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”.请你解释“夏天晒盐,冬天捞碱”的原因.

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:
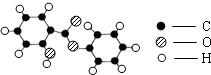 在宏观、微观和符号之间建立联系是化学学科特点.
在宏观、微观和符号之间建立联系是化学学科特点.| 物质 | B | C | D |  ─氢原子 ─氢原子 ─氧原子 ─氧原子 ─碳原子 ─碳原子 |
微观示意图 |
 |
 |
 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?锦江区二模)(一)如图是已破损的维生素C(简写Vc)说明书部分信息.已知维生素C由碳、氢、氧三种元素组成.请回答:
(2012?锦江区二模)(一)如图是已破损的维生素C(简写Vc)说明书部分信息.已知维生素C由碳、氢、氧三种元素组成.请回答:
查看答案和解析>>
科目:初中化学 来源: 题型:

 表示的是
表示的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com