
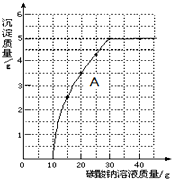
 实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题:
实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题:分析 (1)根据用过量的稀盐酸和大理石制取CO2,反应后的滤液中的溶质是氯化钙和氯化氢,滴滴入碳酸钠溶液,碳酸钠要先与盐酸反应生成氯化钠、水和二氧化碳,盐酸反应完毕后,碳酸钠再与氯化钙反应生成碳酸钙沉淀和氯化钠,图中A点是盐酸已经反应完毕,而氯化钙还没有反应完毕进行解答;
(2)根据沉淀的最大质量可求出原滤液中氯化钙的质量,然后根据溶质的质量分数的计算方法计算质量分数;
(3)根据沉淀的质量即可求碳酸钠的质量,进而求出原滤液中盐酸的质量分数以及反应后的溶液溶质质量分数进行解答.
解答 解:(1)用过量的稀盐酸和大理石制取CO2,反应后的滤液中的溶质是氯化钙和氯化氢,滴滴入碳酸钠溶液,碳酸钠要先与盐酸反应生成氯化钠、水和二氧化碳,盐酸反应完毕后,碳酸钠再与氯化钙反应生成碳酸钙沉淀和氯化钠,图中A点是盐酸已经反应完毕,而氯化钙还没有反应完毕,所以图中A点溶液中的溶质为NaCl、CaCl2;故填:NaCl、CaCl2;
(2)设原滤液中CaCl2的质量为x,消耗碳酸钠的质量为y,生成氯化钠的质量为z.
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 111 100 117
y x 5g z
$\frac{106}{y}=\frac{111}{x}=\frac{100}{5g}=\frac{117}{z}$
x=5.55g
y=5.3g
z=5.85g
故原滤液中氯化钙的质量分数为:$\frac{5.55g}{50g}$×100%=11.1%
碳酸钠溶液的溶质质量分数=$\frac{5.3g}{20g}$×100%=26.5%
(3)设氯化氢的质量为w,生成氯化钠的质量为n,生成二氧化碳的质量为q.
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 73 117 44
10g×26.5% w n q
$\frac{106}{10g×26.5%}=\frac{73}{w}=\frac{117}{n}=\frac{44}{q}$
w=1.825g
n=2.925g
q=1.1g
原滤液中盐酸的质量分数=$\frac{1.825g}{50g}×100%$=3.65%
当所加碳酸钠溶液完全反应时,反应后的溶液溶质质量分数=$\frac{5.85g+2.925g}{50g+30g-5g-1.1g}×100%$=11.87%
答:(2)原滤液中氯化钙的质量分数为3.65%.
(3)原滤液中盐酸的质量分数为3.65%;当所加碳酸钠溶液完全反应时,反应后的溶液溶质质量分数为11.87%.
点评 此题是对物质的性质及图象识别考查题,解题的关键是能对图象有明确的认识,可以较好的培养学生良好的分析问题的能力.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案科目:初中化学 来源: 题型:选择题
| A. | 单质中只含有一种元素,因此只含有一种元素的物质一定是单质 | |
| B. | 金刚石和石墨都是由碳原子构成,所以它们的性质相同 | |
| C. | 离子是带电荷的粒子,所以带电荷的粒子一定是离子 | |
| D. | 点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 常见物质的溶解度(20℃) | ||||
| 物质名称 | 氯酸钾 | 硝酸钾 | 氯化钠 | 蔗糖 |
| 溶解度/克 | 7.4 | 31.6 | 36.0 | 203.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com