
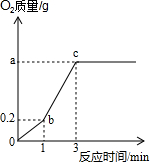
 化学兴趣小组的同学在实验室中用加热4.9g氯酸钾和1.58g高锰酸钾混合物的方法进行了制取氧气的研究,得到如图所示的曲线图.试回答:
化学兴趣小组的同学在实验室中用加热4.9g氯酸钾和1.58g高锰酸钾混合物的方法进行了制取氧气的研究,得到如图所示的曲线图.试回答:
| ||
| △ |
| ||
| 245 |
| 96 |
| 4.9g |
| x |
| 316 |
| 32 |
| 1.58g |
| y |
| 2.98g |
| 4.4g |


科目:初中化学 来源: 题型:阅读理解
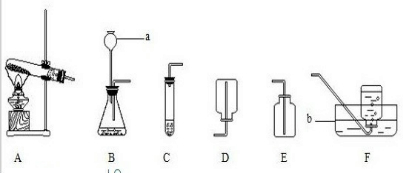
 20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.
20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?太原)某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验:
(2012?太原)某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验:| 实验步骤 | 实验现象 | 结论 |
| 取少量滤渣于试管中,向其中滴加 稀盐酸 稀盐酸 |
没有气泡产生 | 滤渣中没有铁 滤渣中没有铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com