
 ��ͼ��A��B�������ʵ��ܽ�����ߣ��Իش��������⣺
��ͼ��A��B�������ʵ��ܽ�����ߣ��Իش��������⣺���� ���ݹ�����ܽ�����߿��ԣ��ٲ��ij������һ���¶��µ��ܽ�ȣ��Ӷ�ȷ�����ʵ��ܽ��ԣ��ڱȽϲ�ͬ������ͬһ�¶��µ��ܽ�ȴ�С���Ӷ��жϱ�����Һ�����ʵ����������Ĵ�С�����ж����ʵ��ܽ�����¶ȱ仯�ı仯������Ӷ��ж�ͨ�����½ᾧ���������ᾧ�ķ����ﵽ�ᴿ���ʵ�Ŀ�ģ�
��� �⣺��1��ͨ�������ܽ�����߿�֪��t2��ʱ��A���ʵ��ܽ��Ϊ60g�����¶��£�A���ʵ��ܽ�ȴ���B���ʵ��ܽ�ȣ����Էֱ����������ˮ�м���������A��B���ʣ��ܽ�϶����A��
��2��t1��ʱ��A��B���ʵ��ܽ����ȣ�����40g�����Ե�A��B������Һ����������������ͬʱ����Һ���¶���t1�棬���¶��±�����Һ�����ʺ��ܼ���������Ϊ��40g��100g=2��5��
��3��t2��ʱ��B���ʵ��ܽ��С��60g�����Խ�60gB���ʷ���100gˮ�У��γɱ�����Һ��
��4��t2��ʱ��A���ʵ��ܽ����60g��160gA�ı�����Һ�к���60g��A��100gˮ��t1��ʱ��A���ʵ��ܽ����40g����160gA���ʵı�����Һ������t1�棬��������20g��
�ʴ�Ϊ����1��60��A��
��2��t1�棬2��5��
��3�����ͣ�
��4��20��
���� �����ѶȲ��Ǻܴ���Ҫ�����˹�����ܽ����������ʾ�����壬�����ݹ�����ܽ�������������ص����⣬�Ӷ������������⡢��������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
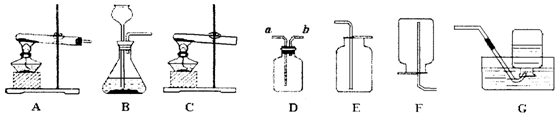
| A�� | ���������ۻ� | |
| B�� | Ũ���᳨�ڷ����ڿ������γɰ��� | |
| C�� | �������ƹ��屩¶�ڿ������������� | |
| D�� | ��ˮɹ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ�����峣���������� | B�� | һ�������������ɱ�ΪҺ̬ | ||
| C�� | ����������ռ78% | D�� | ������̼�������ӿɵ�������ЧӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
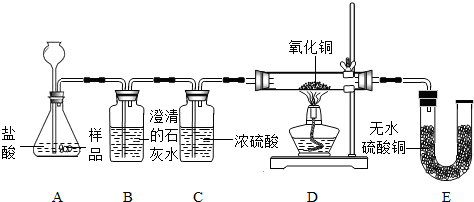
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
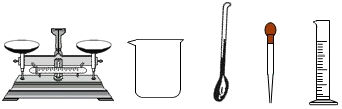
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
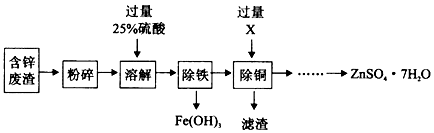
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com