
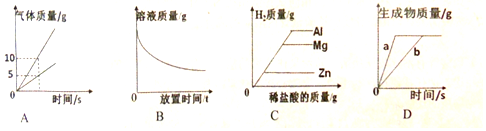
| A. | 电解水产生气体的变化 | |
| B. | 敞口放置于空气中的浓硫酸 | |
| C. | 等质量的镁、铝、锌分别与等质量等浓度的稀盐酸反应 | |
| D. | 用等质量等浓度的过氧化氢溶液制氧气,加MnO2的曲线是b |
分析 A、根据电解水的实验结论可以完成解答;
B、根据硫酸的吸水性分析;
C、根据金属与酸反应时酸的质量与氢气的关系分析;
D、根据催化剂的特点分析判断.
解答 解:A、电解水实验中产生氢气和氧气的质量之比为1:8,故A错;
B、由于浓硫酸具有吸水性,敞口放置于空气中的浓硫酸中溶剂的质量增大,溶质质量不变,故B错;
C、根据金属与酸的反应时产生氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属的质量可知,等质量的镁、铝、锌分别与等质量等浓度的稀盐酸反应生成氢气的多少关系是:铝>镁>锌,故C正确;
D、由于二氧化锰能加快过氧化氢的分解,所以用等质量等浓度的过氧化氢溶液制氧气,反应的时间短,加MnO2的曲线是a,故D错.
故选C.
点评 熟练掌握酸碱盐的化学性质,能够熟练的运用金属的活动性顺序的应用来解答相关题目,知道电解水实验中氢气和氧气的体积比为2:1,而不是质量比.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 非金属材料 | B. | 有机合成材料 | C. | 复合材料 | D. | 金属材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
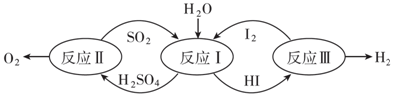
| A. | 反应Ⅰ方程式为:SO2+I2+2H2O=H2SO4+2HI | |
| B. | 反应Ⅱ中的第二步反应中,SO3分解生成S和O2 | |
| C. | 反应Ⅰ属于化合反应,反应Ⅱ、III属于分解反应 | |
| D. | 该生产工艺中最终被消耗的物质是H2O、S和I2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加碘盐、水、纯碱 | B. | 稀有气体、干冰、熟石灰 | ||
| C. | 冰水混合物、液氧、火碱 | D. | 钢、高锰酸钾、氢氧化镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
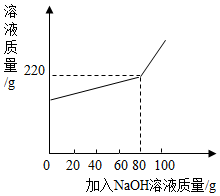 将一定量氯化镁和氯化钠的固体混合物加水配成145.8g的溶液,向所得溶液中加入一定浓度的氢氧化钠溶液,加入氢氧化钠溶液的质量与反应后溶液的质量关系如图.计算:
将一定量氯化镁和氯化钠的固体混合物加水配成145.8g的溶液,向所得溶液中加入一定浓度的氢氧化钠溶液,加入氢氧化钠溶液的质量与反应后溶液的质量关系如图.计算:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
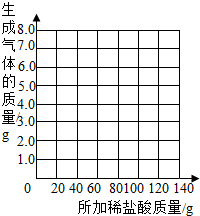
| 加入盐酸的次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 烧杯及所称物质总质量/g | 78.9 | 97.8 | 116.7 | 135.60 | 155.05 | 175.05 | 195.05 |
| 生成气体的质量/g | 1.1 | 2.2 | a | 4.4 | 4.95 | b | -- |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com