
根据下列反应事实写出相应的化学方程式。
(1)氯酸钾(KClO3)在二氧化锰的催化作用下受热分解生成氯化钾和氧气:_____。
(2)Cu和AgNO3溶液反应,生成Cu(NO3)2溶液和Ag:_____。
(3)少量CuSO4溶液滴入NaOH稀溶液中生成Cu(OH)2沉淀和Na2SO4溶液:_____。
(4)一氧化碳和四氧化三铁在高温下反应生成铁和二氧化碳:_____。
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源:江苏省无锡市滨湖区2019届九年级下学期中考二模化学试卷 题型:单选题
2018年夏天,电影《我不是药神》让无数人泪目。片中的格列宁是治疗慢粒白血病的特效药,通用名称为甲磺酸伊马替尼,化学式为C29H31N7O•CH4SO3.下列关于格列宁的说法正确的是( )
A. 格列宁的相对分子质量是589g
B. 一个格列宁分子中有77个原子
C. 格列宁中含有三氧化硫分子
D. 格列宁中碳、氢、氧元素的质量比为30:35:4
查看答案和解析>>
科目:初中化学 来源:广东省惠州市博罗县2019届九年级下学期教学质量监测化学试卷 题型:简答题
菱铁矿(主要成分是FeCO3)是炼铁的原料。现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如下图所示。
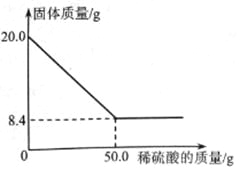
已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O
②菱铁矿中杂质不参加反应,且难溶于水。
请计算:
(1)20.0g菱铁矿中FeCO3的质量为 g。
(2)列式计算所用稀硫酸的溶质质量分数(结果准确到0。1%)
查看答案和解析>>
科目:初中化学 来源:广东省惠州市博罗县2019届九年级下学期教学质量监测化学试卷 题型:单选题
同样是清洁剂,炉具清洁剂有强碱性,而厕所清洁剂则有强酸性,用这两种清洁剂进行实验得到的结果一定有误的是
A. 测得炉具清洁剂pH=13 B. 测得厕所清洁剂pH=8
C. 炉具清洁剂使无色酚酞溶液变红 D. 厕所清洁剂使紫色石蕊溶液变红
查看答案和解析>>
科目:初中化学 来源:广东省惠州市博罗县2019届九年级下学期教学质量监测化学试卷 题型:单选题
根据日常经验和你所学的化学知识,判断下列变化中不属于化学变化的是( )
A. 灯泡发光 B. 燃放烟花 C. 塑料饭盒降解 D. 动物的呼吸作用
查看答案和解析>>
科目:初中化学 来源:山东省荣成市等六校联考2019届八年级下学期期中考试化学试卷 题型:单选题
下列实验中对水的作用解释不正确的是( )
A | B | C | D | |
实验 内容 |
空气中O2量测定 |
铁丝在氧气中燃烧 |
检查气密性 |
收集氧气 |
水的作用 | 通过量筒中水体积变化得出O2体积。 | 防止熔融物溅落下来炸裂集气瓶。 | 降温,便于气 密性检查。 | 排净空气,便于观察何时集满。 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源:江苏省扬州市邗江区2019届九年级下学期第一次模拟考试化学试卷 题型:科学探究题
硫酸是一种重要的化工原料,也是实验室中常用的化学试剂。下面是对硫酸的性质、制取、用途等方面的探究,请你共同参与并回答有关问题。
(探究一)硫酸的性质
(1)探究浓硫酸的某些特性。
①用小木棍蘸取少量浓硫酸,放置一会后,可观察到___。
②浓硫酸的稀释:浓硫酸稀释过程如图1所示,b中盛放的物质是___,a的作用是___。
③兴趣小组把98%的浓硫酸10ml和63.3%的硫酸溶液约20mL分别放入两个相同的小烧杯中,称量、观察、记录、分析,根据室温环境下实验的数据绘成的曲线如图2.由图2曲线你能得到的实验结论:_____(写两点)。
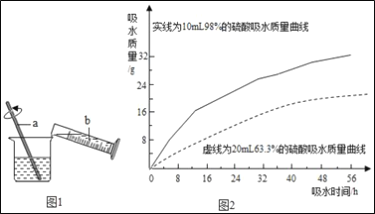
(2)探究稀硫酸的化学性质。
如图3将适量的稀硫酸分别加入A~E的五只烧杯中。
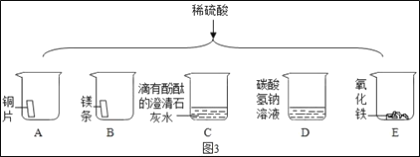
①有产生气泡的是___(填序号,下同);有白色沉淀生成的是___。
②能证明C中发生化学反应的现象是___。
(3)请写出稀硫酸的一种用途___。
(探究二)硫酸的工业制法。
工业上以黄铁矿为原料生产硫酸的工艺流程如图4所示。
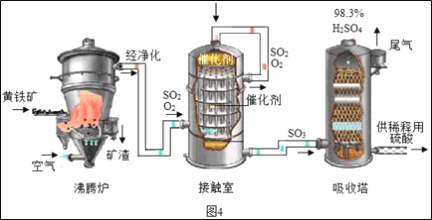
(1)接触室中发生的化学方程式为___。
(2)依据生产硫酸的工艺流程图,下列说法正确的是___(填字母序号)。
A 为使黄铁矿充分燃烧,需将其粉碎 B 催化剂能够提高SO2的反应速率和产量
C 吸收塔中得到的产品为混合物 D 沸腾炉排出的矿渣可供炼铁
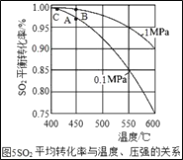
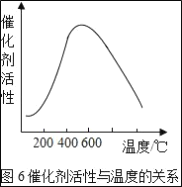
(3)接触室中的SO2平衡转化率与温度及压强的关系如图5所示。催化剂活性与温度的关系见图6.在实际生产中,SO2催化氧化反应的条件选择常压和450℃(对应图中A点),而没有选择SO2转化率更高的B或C点对应的反应条件,其原因分别是___;___。
(探究三)探究某黄铁矿中FeS2的含量。
同学们进行了如下实验探究。
(查阅资料)①4FeS2 +11O2 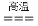 2Fe2O3+8SO2
2Fe2O3+8SO2
②Na2SO3 +H2O2 =Na2SO4 +H2O
(实验探究)
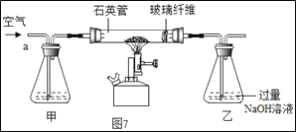
Ⅰ称取1.60g黄铁矿样品放入如图7所示装置(夹持装置省略)的石英管中,从a处不断地缓缓通入空气、高温灼烧石英管中的黄铁矿样品至完全反应。
Ⅱ反应结束后,将乙瓶中的溶液进行如图8处理
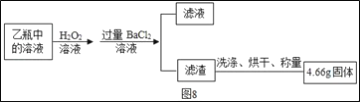
(问题讨论)
(1)I中装置甲瓶内盛放的试剂是氢氧化钠溶液,其作用是___;II中滤液所含的溶质一定有___。
(含量测定)
(2)II中最终得到的4.66g固体是___(填化学式)。
(3)计算该黄铁矿中FeS2的质量分数为___。(写出计算过程)
(交流反思)
(4)如果缺少甲装置,则最终测得FeS2的质量分数将会___(填“偏大”“偏小”“不变”)
(5)如何证明II中所加BaCl2溶液已过量(请简要写出操作方法及现象)___。
查看答案和解析>>
科目:初中化学 来源:山东省济南市章丘市2019届九年级下学期中考二模化学试卷 题型:单选题
向一定量的FeSO4和CuSO4的混合溶液中加入x g锌粉,充分反应后过滤,得滤液和滤渣,向滤渣中加入稀盐酸,有气泡产生。由此判断,下列说法错误的是( )
A. 滤液的颜色呈蓝色
B. 滤液中可能存在Fe2+
C. 滤液中一定含有Zn2+
D. 滤渣中一定含有Fe和Cu,可能含有Zn
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com