
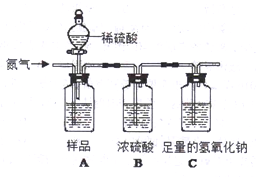
 在实验室,小柯看到一瓶长久放置的氢氧化钠固体样品,他想:这瓶氢氧化钠有无变质呢?于是他和小组同学进行了如下探究:
在实验室,小柯看到一瓶长久放置的氢氧化钠固体样品,他想:这瓶氢氧化钠有无变质呢?于是他和小组同学进行了如下探究:分析 (1)氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠;
碳酸钠溶液和氢氧化钠溶液都是显碱性溶液,都能使酚酞试液变红色;
(2)①二氧化碳能够溶于水,将样品与足量的稀盐酸充分反应,用排水法收集完全反应后的二氧化碳气体设,会导致二氧化碳质量偏小,从而导致由二氧化碳气体的质量来求解出的结果偏小;
②稀硫酸能和氢氧化钠反应生成硫酸钠和水,能和碳酸钠反应生成硫酸钠、水和二氧化碳,根据参加反应的稀硫酸质量无法直接求解;
③碳酸钠和氯化钙反应生成碳酸钙和氯化钠,因此可以将样品与足量的氯化钙溶液反应,将沉淀过滤、洗涤、干燥、称量,由得到的沉淀来求解;
④浓盐酸挥发出的氯化氢能被氢氧化钠溶液吸收,将样品与足量的浓盐酸充分反应,将逸出的气体用NaOH溶液充分吸收,NaOH溶液增加的质量大于二氧化碳气体的质量,会导致根据二氧化碳气体来求解出的结果偏大;
(3)A.把通入的氮气改为空气时,二氧化碳能被氢氧化钠溶液吸收,导致计算结果偏大;
B.稀硫酸过量不影响计算结果;
C.鼓入氮气的时间较长不影响实验结果;
D.省略装置B时,会导致水蒸气进入氢氧化钠溶液中,导致计算结果偏大.
解答 解:(1)取少量固体溶于水,得到无色澄清的溶液,先向溶液中滴加酚酞试液,振荡,再向溶液中滴加过量的氯化钡溶液,如果溶液由无色变成红色,产生白色沉淀,则证明氢氧化钠部分变质.
故填:溶液由无色变成红色,产生白色沉淀.
(2)其他三种方案不能测量的理由是:
①二氧化碳能够溶于水,将样品与足量的稀盐酸充分反应,用排水法收集完全反应后的二氧化碳气体设,会导致二氧化碳质量偏小,从而导致由二氧化碳气体的质量来求解出的结果偏小;
②稀硫酸能和氢氧化钠反应生成硫酸钠和水,能和碳酸钠反应生成硫酸钠、水和二氧化碳,根据参加反应的稀硫酸质量无法直接求解;
④浓盐酸挥发出的氯化氢能被氢氧化钠溶液吸收,将样品与足量的浓盐酸充分反应,将逸出的气体用NaOH溶液充分吸收,NaOH溶液增加的质量大于二氧化碳气体的质量,会导致根据二氧化碳气体来求解出的结果偏大;
设碳酸钠质量为x,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100
x 10g
$\frac{106}{x}$=$\frac{100}{10g}$,
x=10.6g,
样品中所含碳酸钠的质量分数为:$\frac{10.6g}{20g}$×100%=53%,
故答案为:①二氧化碳能够溶于水,将样品与足量的稀盐酸充分反应,用排水法收集完全反应后的二氧化碳气体设,会导致二氧化碳质量偏小,从而导致由二氧化碳气体的质量来求解出的结果偏小;
②稀硫酸能和氢氧化钠反应生成硫酸钠和水,能和碳酸钠反应生成硫酸钠、水和二氧化碳,根据参加反应的稀硫酸质量无法直接求解;
④浓盐酸挥发出的氯化氢能被氢氧化钠溶液吸收,将样品与足量的浓盐酸充分反应,将逸出的气体用NaOH溶液充分吸收,NaOH溶液增加的质量大于二氧化碳气体的质量,会导致根据二氧化碳气体来求解出的结果偏大;53%.
(3)A.把通入的氮气改为空气时,二氧化碳能被氢氧化钠溶液吸收,导致计算结果偏大;
B.稀硫酸过量不影响计算结果;
C.鼓入氮气的时间较长不影响实验结果;
D.省略装置B时,会导致水蒸气进入氢氧化钠溶液中,导致计算结果偏大.
故填:AD.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 智能训练练测考系列答案
智能训练练测考系列答案科目:初中化学 来源: 题型:计算题
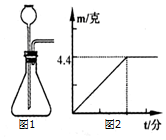 实验室用图1气体发生装置来制取二氧化碳,老师给小李提供了石灰石、无标签的稀盐酸和稀硫酸水溶液各一瓶.
实验室用图1气体发生装置来制取二氧化碳,老师给小李提供了石灰石、无标签的稀盐酸和稀硫酸水溶液各一瓶.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
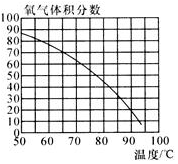 小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:
小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究:| 第一组 | 第二组 | 第第三组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | l0 | 20 | 30 | 40 | 50 | 3l | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | 质量(克) |
| 坩埚+硫酸铜晶体 | 45.5 |
| 坩埚+无水硫酸铜 | 36.5 |
| 坩埚 | 20.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
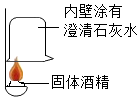 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.| 方案 | 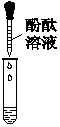 |  |
| 现象 | 溶液变红 | 产生白色沉淀 |
| 结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
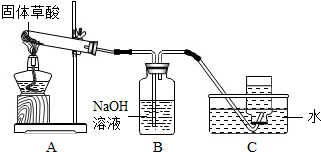
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 将甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图相符合的是( )
将甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图相符合的是( ) | 选项 | 甲物质 | 乙物质 | Y轴表示的含义 |
| A | 碳酸钙 | 稀盐酸 | H2O的质量 |
| B | T℃的水 | 硝酸钾 | T℃硝酸钾的溶解度 |
| C | 铁与铜的混合粉末 | 硝酸铜 | 混合粉末中铜的质量 |
| D | 饱和石灰水 | 生石灰 | 溶液的质量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com