【答案】
分析:利用四种实验用品中①带火星的木条与③澄清石灰水的特殊性,可判断四种实验用品中的任意一种都可用来鉴别的两种常见气体;
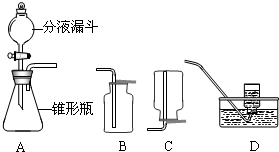
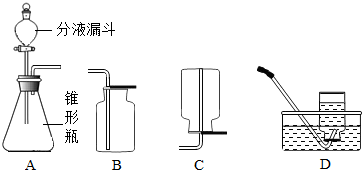
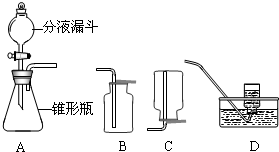
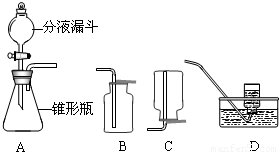
(1)①由装置用于固体与液体不需加热制取气体的适用条件,判断制取气体的反应原理,写出反应的化学方程式;
②根据气体的密度、溶解性决定气体的收集方法,由两种气体的密度大于空气,氧气不易溶于水而二氧化碳能溶于水的性质,解答关于收集的问题;
③澄清的石灰水能与二氧化碳反应而不能与氧气反应,因此,写出二氧化碳与石灰水反应的化学方程式;
④根据反应剧烈程度与反应物的量相关的特点,为控制装置A中很剧烈的反应,可采取控制反应物加入量实现;
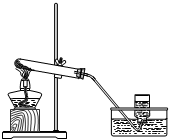
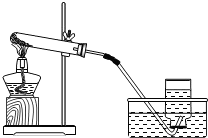
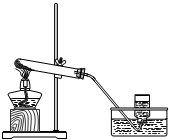
(2)①根据该装置适用于对固体加热制取气体的特点,判断制取气体的反应原理,写出反应的化学方程式;
②根据实验室利用该装置制取氧气时的操作要点及注意事项,对操作过程进行排序.
解答:解:带火星的木条用于检验氧气,而澄清石灰水用来检验二氧化碳,因此,可判断四种实验用品中的任意一种都可用来鉴别的两种常见气体为氧气和二氧化碳;
(1)①该装置用使用双氧水在二氧化碳催化下制取氧气,化学方程式为2H
2O
2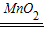
2H
2O+O
2↑;也可用于碳酸钙与盐酸反应制取二氧化碳,化学方程式为CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;
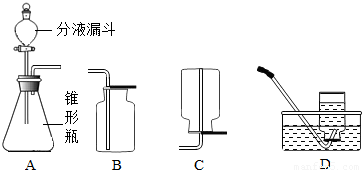
②装置B为向上排气法收集气体,氧气、二氧化碳的密度都大于空气,都可采取此法收集;而二氧化碳能溶于水,不能采取D排水法收集;而C装置为向下排气法收集气体,两种气体密度均大于空气,因此都不适用于C装置的收集方法;
③二氧化碳与石灰水中的氢氧化钙反应,生成碳酸钙沉淀和水,化学方程式为Ca(OH)
2+CO
2=CaCO
3↓+H
2O;
④可采取控制液体的滴加速度的方法实现控制装置A中反应过于剧烈的情况,而用体积较小的锥形瓶、或加热的方法都会使反应更加剧烈;
(2)①利用该装置,可加热分解高锰酸钾或氯酸钾制取氧气,化学方程式为2KMnO
4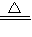
K
2MnO
4+MnO
2+O
2↑或2KClO
3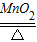
2KCl+3O
2↑;
②使用该装置进行制取氧气时,首先应E检查装置气密性,然后A将药品装入试管并塞上塞子,接下来D用铁架台和铁夹把盛有药品的试管固定起来,C点燃酒精灯先给试管预热再集中给药品加热,F气泡连续且均匀放出来时收集一瓶气体,G将导气管从水槽内取出来,最后B移开并熄灭酒精灯;故操作顺序应为EADCFGB;
故答案为:氧气;二氧化碳;
(1)①2H
2O
2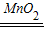
2H
2O+O
2↑;CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;
②CO
2、O
2;D;它们的密度都比空气的密度大;
③Ca(OH)
2+CO
2=CaCO
3↓+H
2O;
④A;
(2)①2KMnO
4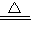
K
2MnO
4+MnO
2+O
2↑或2KClO
3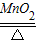
2KCl+3O
2↑;
②EADCFGB.
点评:熟练掌握实验室制氧气、二氧化碳的原理、装置、操作,是解答此题所必须具备的基础,否则面对此类无具备目的习题将会一筹莫展.

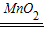 2H2O+O2↑;也可用于碳酸钙与盐酸反应制取二氧化碳,化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
2H2O+O2↑;也可用于碳酸钙与盐酸反应制取二氧化碳,化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;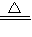 K2MnO4+MnO2+O2↑或2KClO3
K2MnO4+MnO2+O2↑或2KClO3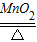 2KCl+3O2↑;
2KCl+3O2↑;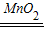 2H2O+O2↑;CaCO3+2HCl=CaCl2+H2O+CO2↑;
2H2O+O2↑;CaCO3+2HCl=CaCl2+H2O+CO2↑;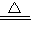 K2MnO4+MnO2+O2↑或2KClO3
K2MnO4+MnO2+O2↑或2KClO3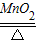 2KCl+3O2↑;
2KCl+3O2↑;