
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②⑤ | C. | ①③④ | D. | ③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
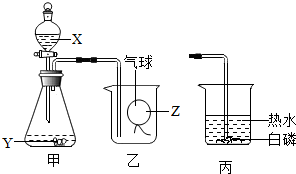 丽丽同学利用如图所示的装置做了一个趣味实验:开始时气球沉于烧杯底部,气球内气体为一种单质(气球的质量忽略不计).打开分液漏斗活塞后,一会后气球从烧杯底部慢慢浮了起来,最后悬浮烧杯口.
丽丽同学利用如图所示的装置做了一个趣味实验:开始时气球沉于烧杯底部,气球内气体为一种单质(气球的质量忽略不计).打开分液漏斗活塞后,一会后气球从烧杯底部慢慢浮了起来,最后悬浮烧杯口.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化合物一定是纯净物,则纯净物一定是化合物 | |
| B. | 酸能电离产生H+,则能电离产生H+的一定是酸 | |
| C. | 氢气在氧气中燃烧生成水要释放能量,则水分解生成氢气和氧气需吸收能量 | |
| D. | 有氧得失的为氧化还原反应,氧化还原反应必须有氧得失 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com