
某化学兴趣小组学习酸碱中和反应后,对稀盐酸与氢氧化钠溶液混合后的有关问题,进行了如下探究,请你一起参与他们的探究。
【提出问题】氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】
甲同学猜想:溶质有NaCl、HCl、NaOH
乙同学猜想:溶质只有NaCl
丙同学猜想:溶质有NaCl、HCl
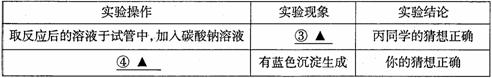
你的猜想:溶质有 ① .(填化学式)
乙同学认为甲同学的猜想是错误的,理由是 ② 。
【实验设计及验证】请你将下列实验报告填写完整:
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:初中化学 来源: 题型:
“低碳生活”、“低碳经济”、“碳减排”等日常出现在电视新闻或报纸上,其中关于“低碳生活”中的“低碳”是指 ( )
A.生活中不用含碳的物质 B.尽量减少含碳物质的排放和浪费
B.停止含碳矿物的开采和加工 D.禁止使用煤炭、石油
查看答案和解析>>
科目:初中化学 来源: 题型:
某化学兴趣小组的同学在教师的指导下,正确完成如下图所示的两实验。已知所用实验装置气密性良好。


实验一 实验二
关于该实验有如下说法:①红磷熄灭并冷却后才能打开弹簧夹;②点燃酒精灯加热铜丝,可观察到铜丝由红色变成黑色;③停止加热后即可读出注射器内气体体积约为24mL;④实验取用铜丝的多少不会影响实验结果;⑤两个实验均能证明空气是混合物;⑥两个实验均能证明空气中约含1/5体积的氧气。
其中正确说法的个数有( )
A.2个 B.3个 C.4个 D.5个
查看答案和解析>>
科目:初中化学 来源: 题型:
化学兴趣小组设计的创新实验是“火龙生字”。在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1)。用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(间图2)。在场的同学对此产生了浓厚的兴趣,并进行了如下探究:
【提出问题】为甚附有硝酸钾的白纸更容易燃烧?
【查阅资料】硝酸钾受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质。
【猜想与假设】对于生成的是什么气体,四位同学有如下猜想:
甲:二氧化氮;乙:氮气;丙:氧气;丁:氢气。
同学丙指出不可能是二氧化氮、氢气,理由是: ; 。
【进行实验】四位同学设计了实验对同学丙的猜想进行了验证,他们的操作方法是:
,观察到的现象是 ,说明同学丙的猜想正确。
硝酸钾分解的化学方程式是 :
【解释与结论】白纸上写过字的地方更容易燃烧的原因是: 。
【反思与评价】为什么要用“硝酸钾的热饱和溶液”书写文字?
已知硝酸钾在不同温度时的溶解度如下表:
| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 31.6 | 63.9 | 110 | 169 | 246 |
你对上述问题的解释: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
某校学习小组准备探究气体的测定和数据处理方法
【提出问题】
如何利用石灰石(主要成分为CaCO3)与稀盐酸反应来测定生成的CO2的质量和体积,并处理数据。
【实验设计】
通过下列两个实验分别测定CO2的质量和体积:

【分析与表达】
(1)上述两个实验中,反应的化学方程式是_______________________。
(2)实验Ⅰ中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是___________________________________________。
(3)实验Ⅱ中,先连接好装置,再_______(填操作名称),然后装好药品,最后将10 mL稀盐酸快速推入到烧瓶中,若稀盐酸是缓慢推入的,则可能造成的后果是______。
【记录与处理】
(4)已知实验Ⅰ反应前的总质量[m(大烧杯+石灰石粉末)+m(小烧杯+稀硫酸)],要计算生成的CO2的质量,至少还需要的数据是_______(填序号)
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后的剩余物)
(5)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定)
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/mL | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
①  根据以上实验过程和数据综合分析,最终生成CO2
根据以上实验过程和数据综合分析,最终生成CO2
的体积是______mL,理由是____________。
②根据你的认识,在坐标图中绘制出0~10min生成
CO2体积随时间变化的曲线。
【反思与评价】
(1)经过分析,你认为实验Ⅰ的优点是________,实验Ⅱ
的优点是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体。在反应过程中,溶液的温度也先随之升高,最后下降到室温。于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”。测得实验数据如下:
某金属与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10 mL | 60 mL |
| 10% | 20℃ | 19 mL | 118 mL |
| 15% | 20℃ | 28 mL | 175 mL |
| 5% | 35℃ | 28 mL | 60 mL |
| 10% | 35℃ | 72 mL | 118 mL |
| 15% | 35℃ | 103 mL | 175 mL |
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有 ▲ 、 ▲ 。
(2)可以通过比较 ▲ 实验数据来确定金属和酸反应的快慢。
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢。请分析原因。 ▲ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
某兴趣小组对“蜡烛燃烧的产物”进行探究。
【查阅资料】蜡烛的主要成分是石蜡,石蜡由碳、氢两种元素组成。
【作出猜想】蜡烛燃烧的产物是二氧化碳和水。
【实验验证】(1)用干冷的小烧杯罩在蜡烛火焰上,观察到 ,证明有水生成。
(2)用涂有饱和石灰水的小烧杯罩在火焰上,石灰水变浑浊,证明有二氧化碳生成,二氧化碳和石灰水反应的化学方程式为 。
小明提出质疑:石灰水变浑浊不一定是生成了碳酸钙,还可能是饱和石灰水受热后 ,析出了氢氧化钙。
同学们又用图20所示的装置进行实验,1分钟后,提起锥形瓶,翻转后注入20mL饱和石灰水,加塞、振荡,观察到石灰水变浑浊,确定有二氧化碳生成。

实验中小明观察到一个意外现象:锥形瓶内壁上有少量黑色物质。
【交流讨论】经分析,同学们一致认为是石蜡不充分燃烧生成的 。由此他们猜想还可能生成一氧化碳。
为验证一氧化碳,他们设计了如图21所示的实验。

【实验验证】(1)实验前,先在玻璃管的中部放入一团棉花,其目的是 。
(2)用酒精灯加热b端的糊状物,一段时间后,观察到黑色物质变成红色,证明蜡烛部充分燃烧有一氧化碳生成。
(4)为防止玻璃管中的红色物质又被氧化成黑色,接下来的操作是: 。
【拓展应用】含碳燃料不充分燃烧会生成一氧化碳等物质,浪费资源,且污染空气。为使其充分燃烧,应采取的措施是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
化学课堂上要学习碱的性质,老师让两位为同学和他共同实验,要求两位同学分别向澄清的石灰水和氢氧化钠的溶液里吹起,如图①②所示,老师告诉同学们,呼出的气体中只有二氧化碳能和氢氧化钠溶液和澄清的石灰水反应

同学们吹起后观察到①澄清石灰水变浑浊,②中氢氧化钠溶液无明显现象.。观察实验现象后老师问,通过实脸现象的观察,检验二氧化碳气体应该使用________.针对②中的情况师生共同开始探究之旅.
(1)小明设计了如图所示的③、④两个实验.
实验现象:③中软塑料瓶变瘪,④中______________
(2)小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低。小光同学却对此提出质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是___________
(3)小光设计的是通过检验生成物来验证猜想,请帮他填写实验报告.
| 实验步步骤 | 实验现象 | 实验结论 |
| 取③实验后的溶液少许, 再向其中加人____ | ______ | 验证了二氧化碳和氮氧化 钠溶液反应. |
【实验结论】二氧化碳和氢氧化钠溶液发生了化学反应。
【反思拓展】探究结束老师说,通过此探究实验我们发现,对于没有明显现象的化学反应,可以从不同的角度证明反应的发生,这些角度可以是:①通过检验反应物减少证明反应发生;②通过_________________证明反应的发生。
查看答案和解析>>
科目:初中化学 来源: 题型:
纳米级Cu2O因具有优良的催化性能备受关注,某
兴趣小组同学在《培养中学生基本科学素养的化学实验教学研究》课题组老师的指导下开展
了系列研究.
Ⅰ纳米级Cu2O的用途研究
【查阅资料】
①NH3是一种有刺激性气味的气体,在高浓度氧气中才能燃烧,生成氮气和水。
① 在纳米级Cu2O的催化作用下,氮气和氧气在一定温度下发生以下化学反应:
4 NH3+5O2==4NO+6H2O 4 NH3+3O2==2N2+6H2O
 工业上用NO制备硝酸、氮肥等化工产品。
工业上用NO制备硝酸、氮肥等化工产品。
【实验1】
设计右图的实验装置验证氮气在氧气中燃烧:将过量的氧气与氮气分别从a,b两管进气口通入,并在b管上端点燃氨气。实验中需先通入氧气,后通入氨气,理由是________
【实验2】
设计下图实验装置,并对生成物进行成分分析:

 根据气体成分分析数据,同学们绘制了曲线图(见右图),发现在纳米级Cu2O的催化作用下,300℃可以生成______为主。若利用后续处理装置模拟硝酸的工业制法,最好将电热丝的温度控制在____________℃左右。
根据气体成分分析数据,同学们绘制了曲线图(见右图),发现在纳米级Cu2O的催化作用下,300℃可以生成______为主。若利用后续处理装置模拟硝酸的工业制法,最好将电热丝的温度控制在____________℃左右。
Ⅱ纳米级Cu2O的制备研究
利用某些特殊的细菌,在一定条件下将某岩石中的不溶性硫化铜(CuS)转化为可溶性硫化铜,进而制得纳米级Cu2O,其流程如下:

(1)在细菌作用下,岩石中的硫化铜(CuS)与空气中的氧气反应生成硫酸铜,反应的化学方程式为:_______________________
(2)③中观察到的现象是__________________
(3)在加热条件下,用液态肼(N2H4)还原新制Cu(OH)2生成Cu2O、N2和H2O,反应的化学方程式为_________________________________,Cu2O中铜元素的化合价是_________
(4)经测定该岩石由硫化铜(CuS)和其他不含铜元素的物质组成.现用1000g该岩石制得21.6g纯氧化亚铜(Cu2O),该纯氧化亚铜(Cu2O)中铜元素的质量是_____g。若制得氧化亚铜(Cu2O)的过程中,铜元素的总损耗为25%,通过计算确定该岩石中硫化铜(CuS)的质量分数(请写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com