
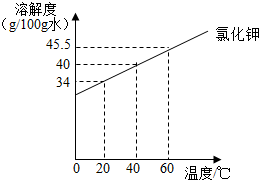
 根据下表实验,回答相关问题
根据下表实验,回答相关问题| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 在盛有100g水的烧杯中,加入25g氯化钾,搅拌,恢复到20℃. | 全部溶解 |
| Ⅱ | 再加Xg氯化钾,搅拌,恢复到20℃,恰好饱和. | 全部溶解 |
| Ⅲ | 再加6g氯化钾,搅拌,恢复到20℃ | 固体不溶 |
| Ⅳ | 加热 | 全部溶解 |
| Ⅴ | 冷却至20℃ | ________ |
| 实验步骤 | 实验现象与结论 |
| 取样,加入________ | ________,是碳酸钾溶液 |
| 实验步骤 | 实验现象与结论 |
| 取样,加入 BaCl2或Ba(NO3)2 | 产生白色沉淀,是碳酸钾溶液 |


科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 反应时间t/s | t0 | t1 | t2 | t3 | t5 | t6 |
| 气体质量m/g | 0 | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 温室效应已引起全球广泛关注,某校研究小组的同学为了研究空气中CO2含量对空气温度的影响,进行了下列实验:
温室效应已引起全球广泛关注,某校研究小组的同学为了研究空气中CO2含量对空气温度的影响,进行了下列实验:| 时间/min 温度/℃ CO2含量 |
起始 | 1 | 2 | 3 | 4 | 5 |
| 全部空气 | 23.0 | 23.3 | 23.9 | 24.6 | 25.0 | 25.5 |
| 10% | 23.0 | 23.5 | 24.2 | 25.0 | 26.0 | 27.0 |
| 20% | 23.0 | 24.0 | 24.5 | 25.6 | 26.5 | 27.5 |
| 30% | 23.0 | 24.5 | 25.0 | 26.2 | 27.5 | 29.0 |
| 100% | 23.0 | 30.0 | 33.0 | 35.6 | 37.0 | 39.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:
温室效应已引起全球广泛关注。某校研究小组的同学在“我与化学”活动中,为了研究CO2气体对空气温度的影响,进行了下列实验:
实验一,制取研究所需的CO2气体
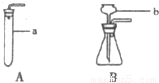
实验室可用下列A、B装置制取CO2
(1)写出下列装置中仪器的名称:a ,b 。
(2)与A装置相比较,B装置的优点是便于在反应过程中 ;
实验二、探究光照条件下CO2气体对空气温度是否有影响
步骤1:用5个规格相同的塑料矿泉水瓶分别收集1瓶空气、1瓶CO2以及3瓶CO2含量分别为10%、20%、30%的空气和CO2的混合气体,并用带温度计的胶塞塞紧瓶口;
2.把上述装有气体的矿泉水瓶放到电灯下照射,每隔1分钟记录一次温度,实验数据如下表:
|
CO2含量 | 起始 | 1 | 2 | 3 | 4 | 5 |
| 全部空气 | 23.0 | 23.3 | 23.9 | 24.6 | 25.0 | 25.5 |
| 10% | 23.0 | 23.5 | 24.2 | 25.0 | 26.0 | 27.0 |
| 20% | 23.0 | 24.0 | 24.5 | 25.5 | 26.5 | 27.5 |
| 30% | 23.0 | 24.5 | 25.0 | 26.2 | 27.5 | 29.0 |
| 100% | 23.0 | 30.0 | 33.0 | 35.6 | 37.0 | 39.5 |
回答下列问题:
(3)仔细阅读表中数据,该实验可以得出的结论是:
① ;
② 。
(4)根据上述数据推测,在相同条件下,当CO2气体含量为25%时,温度达到25.5℃所需要的时间范围为 min。
查看答案和解析>>
科目:初中化学 来源:2007-2008学年山东省烟台市莱州市八年级(下)期末化学试卷(解析版) 题型:解答题
| 时间/min 温度/℃ CO2含量 | 起始 | 1 | 2 | 3 | 4 | 5 |
| 全部空气 | 23.0 | 23.3 | 23.9 | 24.6 | 25.0 | 25.5 |
| 10% | 23.0 | 23.5 | 24.2 | 25.0 | 26.0 | 27.0 |
| 20% | 23.0 | 24.0 | 24.5 | 25.6 | 26.5 | 27.5 |
| 30% | 23.0 | 24.5 | 25.0 | 26.2 | 27.5 | 29.0 |
| 100% | 23.0 | 30.0 | 33.0 | 35.6 | 37.0 | 39.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com