
某研究性学习小组为测定铜锌合金中铜的质量分数,进行如下实验:取合金10g,向其中不断加入稀硫酸,产生的气体与所加稀硫酸的质量关系如图所示。
求:①稀硫酸中溶质的质量分数。
②合金中铜的质量分数。
解:由图示可知,当加入20g稀硫酸时,合金中的锌恰好反应完全,产生0.1g氢气
设参加反应的硫酸的质量为m,合金中锌的质量为n
Zn + H2SO4 == ZnSO4 + H2↑ ┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅(1分)
65 98 2 ┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅(1分)
n m 0.1g ┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅(1分)
98 / m == 2 /0.1 ┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅(1分)
m == 4.9 g ┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅(1分)
①稀硫酸的溶质质量分数为:(4.9g / 20g)×100% == 24.5% ┅┅(1分)
65 / n== 2 / 0.1g ┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅(1分)
n == 3.25 g ┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅┅(1分)
②合金中铜的质量为:10g – 3.25g == 6.75g ┅┅┅┅┅┅┅┅(1分)
合金中铜的质量分数为:(6.75g / 10g)×100% == 67.5% ┅┅┅(1分)
答:稀硫酸的质量分数为24.5%,合金中铜的质量分数为67.5%。
解析:略


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:初中化学 来源: 题型:
| 反应前 | 反应后 |
| C装置及药品总质量:87,6g | C装置及药品总质量:89,4g |
| D装置及药品总质量:74,7g | D装置及药品总质量:83,5g |
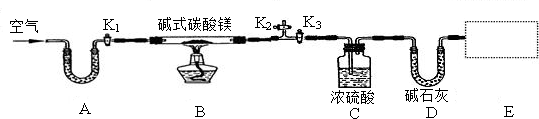
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
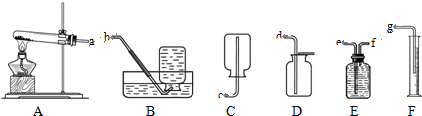
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2011-2012年江苏省扬州市宝应县城北初中九年级(下)化学假期作业(6月份)(解析版) 题型:解答题
| 反应前 | 反应后 |
| C装置及药品总质量:87,6g | C装置及药品总质量:89,4g |
| D装置及药品总质量:74,7g | D装置及药品总质量:83,5g |
查看答案和解析>>
科目:初中化学 来源:2012年江苏省扬州市宝应县城北中学中考化学冲刺试卷(4)(解析版) 题型:解答题
| 反应前 | 反应后 |
| C装置及药品总质量:87,6g | C装置及药品总质量:89,4g |
| D装置及药品总质量:74,7g | D装置及药品总质量:83,5g |
查看答案和解析>>
科目:初中化学 来源:2011年江苏省扬州市维扬区梅苑双语学校中考化学二模试卷(解析版) 题型:解答题
| 反应前 | 反应后 |
| C装置及药品总质量:87,6g | C装置及药品总质量:89,4g |
| D装置及药品总质量:74,7g | D装置及药品总质量:83,5g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com