

分析 根据已有的物质的性质结合物质间反应的化学方程式以及反应的实验现象进行分析解答即可.
解答 解:(1)氧化钙和水反应生成了氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;
(2)②根据题意可以知道在滤液中只有氢氧化钙能够溶于水,所以反应的化学方程式是:
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(3)③滤液中有氢氧化钙显碱性,滴加无色酚酞溶液,溶液由无色变成红色,再滴加过量的稀盐酸,稀盐酸和氢氧化钙反应,氢氧化钙被全部消耗,溶液呈酸性,故溶液由红色变成无色;
(4)向滤液中通入适量二氧化碳若观察到滤液变浑浊,则说明氢氧化钙和二氧化碳反应生成碳酸钙,混合物B中含有碳酸钙,可能还有氢氧化钙;由②知,滴加碳酸钠可以生成碳酸钙沉淀和氢氧化钠,故C中一定有碳酸钙沉淀和氢氧化钠,可能有氢氧化钙或碳酸钠,由③知,滴加无色酚酞溶液,再加过量的稀盐酸,故D中有氯化钙和剩余的氯化氢,将混合物B、C、D倒入一个洁净的烧杯中,发现烧杯中有白色沉淀且上层清液呈红色,说明溶液碱显性碱性,溶质可能是氢氧化钠、氢氧化钙,向滤液E中滴加CaCl2溶有液,有白色沉淀生成,说明溶液中有碳酸钠,有碳酸钠就没有氢氧化钙,由此可知滤液E中的溶质可能是NaCl、Na2CO3或NaCl、Na2CO3、NaOH;
得到的1g滤渣是由氢氧化钙反应生成的,设氢氧化钙的质量是x,则根据反应前后钙原子个数守恒可以有:
Ca(OH)2-------CaCO3
74 100
x 1g
$\frac{74}{x}=\frac{100}{1g}$
x=0.74g
0.75g样品中含有0.1g不溶于水的碳酸钙,得到的滤液中含有氢氧化钙0.74g,而样品溶于水时有热量放出,故样品中一定含有氧化钙,如果0.74g全部是氧化钙,则达到氢氧化钙的质量一定大于0.74g,故样品中含有氧化钙、氢氧化钙和碳酸钙,
答案:
(1)CaO+H2O=Ca(OH)2
(2)Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
(3)滴加无色酚酞溶液,溶液由无色变成红色;再滴加稀盐酸,溶液由红色变成无色
(4)NaCl、Na2CO3、酚酞或NaCl、Na2CO3、NaOH、酚酞
原样品成分:CaO、Ca(OH)2、CaCO3
点评 本题考查的是常见的碱以及盐的有关性质,完成此题,可以依据已有的物质的性质进行.


科目:初中化学 来源: 题型:解答题
 如图是某胃药标签的部分内容.小明同学测定该药品中NaHCO3含量的过程如下:取5g该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7时(已知药品中的其它成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5克.称得反应后烧杯内物质的总质量为64.3克.
如图是某胃药标签的部分内容.小明同学测定该药品中NaHCO3含量的过程如下:取5g该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7时(已知药品中的其它成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5克.称得反应后烧杯内物质的总质量为64.3克.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | Cu粉 | Fe粉 | 用磁铁吸出 |
| B | FeCl2溶液 | CuCl2 | 加过量Fe粉、过滤 |
| C | KOH | K2CO3 | 滴入足量稀盐酸至不再产生气泡 |
| D | MnO2固体 | KCl | 加足量水溶解、过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 据报道:5月9日上午10时许,位于铁西新区宁官附近的某淀粉厂发生粉尘爆炸.淀粉加工厂的车间里若悬浮着较多的淀粉,遇明火就有发生爆炸的危险.下面是模拟粉末爆炸实验:
据报道:5月9日上午10时许,位于铁西新区宁官附近的某淀粉厂发生粉尘爆炸.淀粉加工厂的车间里若悬浮着较多的淀粉,遇明火就有发生爆炸的危险.下面是模拟粉末爆炸实验:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 用于治疗流感的抗病毒药物“达菲”可以有效地预防和治疗甲型H1N1流感.从烹调香料八角中提取到的莽草酸是制取“达菲”的主要原料,如图是莽草酸的一些基本性质.请回答:
用于治疗流感的抗病毒药物“达菲”可以有效地预防和治疗甲型H1N1流感.从烹调香料八角中提取到的莽草酸是制取“达菲”的主要原料,如图是莽草酸的一些基本性质.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | 稀盐酸 | 硫酸 | 过量氢氧化钡溶液 | 过滤 |
| B | KCl | MnO2 | 适量的水 | 加水溶解、过滤、洗涤、干燥 |
| C | 铁 | 铁锈 | 过量硫酸 | 过滤、洗涤 |
| D | 氧气 | 水蒸气 | 足量氢氧化钠固体 | 通过盛有氢氧化钠的装置 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  向稀硫酸中加入铁粉 | |
| B. | 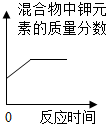 充分加热氯酸钾和二氧化锰的混合物 | |
| C. |  向盐酸中加水稀释 | |
| D. |  向硫酸铜和硫酸混合溶液中滴入氢氧化钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com