
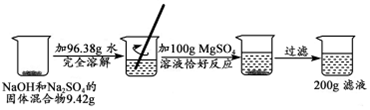
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了氢氧化镁,所以可以求算氢氧化镁的质量,根据氢氧化镁的质量和对应的化学方程式求算硫酸钠和氢氧化钠的质量,进而求算对应的质量分数.
解答 解:根据质量守恒定律可得,生成的沉淀氢氧化镁的质量为9.42g+96.38g+100g-200g=5.8g
设混合物中氢氧化钠的质量为x,生成的硫酸钠的质量为y
2NaOH+MgSO4═Na2SO4+Mg(OH)2↓
80 142 58
x y 5.8g
$\frac{80}{x}$=$\frac{142}{y}$=$\frac{58}{5.8g}$
x=8g
y=14.2g
最终所得溶液的硫酸钠的质量分数为$\frac{14.2g+9.42g-8g}{200g}$×100%=7.81%
由于钠元素质量不变,所以原固体混合物中钠元素的质量和最终的得到的硫酸钠中的钠元素的质量,所以钠元素的质量为(14.2g+9.42g-8g)×$\frac{23×2}{142}$×100%=5.06g.
答:(1)实验过程中,产生沉淀的质量为 5.8g;
(2)最终所得溶液的溶质质量分数为7.81%;
(3)原固体混合物中钠元素的质量为 5.06g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:选择题
| A. | HCl | B. | HClO | C. | HClO3 | D. | HClO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
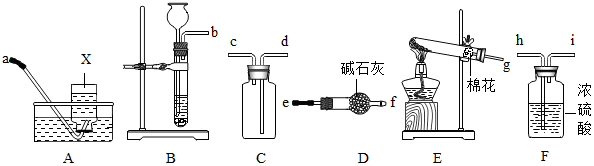
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 易变成分(浓度cm3/m3) | 变化的原因 |
| 二氧化碳 约300(约占空气的0.03%) | |
| 水蒸气约290(约占空气的0.03%) | |
| 甲烷约1.0-1.2t | 天然气泄露 |
| 氮的氧化物约0.52 | 化石燃料的燃烧 |
| 臭氧0.01-0.04 | 含氟化合物的使用 |
| 硫的化合物:二氧化硫、硫化氢等 | 化石燃料的燃烧等 |
| 一氧化碳 | 汽车尾气等 |
| 合计:0.06% |
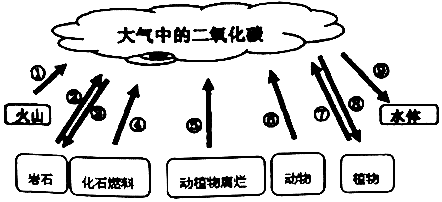
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

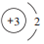 ,该粒子是C.
,该粒子是C.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com