
| 反应时间/mim | 1 | 5 | 8 | 10 | 13 | 15 |
| 实验现象 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 少量气泡 | 反应停止铝条有剩余 |
分析 根据探究影响金属与酸反应的影响因素,铝是较活泼金属,决定了铝与硫酸反应易发生,就是因为铝活泼,也易被空气中的氧气氧化,表面存在氧化层,所以该反应的开始阶段时氧化铝与硫酸反应,随着氧化铝的减少,铝与硫酸接触面积增大,反应加快,后来硫酸的质量分数变小,反应减慢,直到反应停止进行分析.
解答 解:由表中实验现象的记录可知,反应的开始阶段是氧化铝和硫酸反应,随氧化铝的减少,铝与硫酸接触的面积增大,气泡增大,反应在加快,但又随硫酸质量分数的减小,反应变慢,气泡开始减少,氧化铝和硫酸反应生成硫酸铝和水,铝和硫酸反应生成硫酸铝和氢气,化学方程式为:Al2O3+3H2SO4=Al2(SO4)3+3H2O,2Al+3H2SO4=Al2(SO4)3+3H2↑.
故答案为:铝易被空气中的氧气氧化,在铝条表面生成一层致密的氧化物保护膜,将铝条放入稀硫酸中,稀硫酸与铝条表面的氧化铝反应,所以气泡较少;随着氧化铝的减少,铝与硫酸接触面积增大,气泡逐渐增加并达到反应最快;后来硫酸的质量分数越来越小,反应速率减慢,直至停止,Al2O3+3H2SO4=Al2(SO4)3+3H2O,2Al+3H2SO4=Al2(SO4)3+3H2↑.
点评 本题考查影响反应快慢的主要因素是反应物本身的性质,如铝是较活泼金属,则与硫酸反应的就较快;本题还可以看出质量分数也影响反应的快慢.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:初中化学 来源: 题型:解答题
 石墨烯是“新材料之王”
石墨烯是“新材料之王”查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
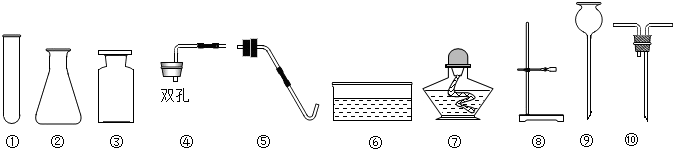
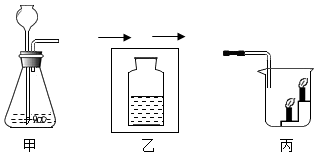
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 金属氧化物 | Fe2O3 | Al2O3 | MgO |
| 开始反应的温度(℃) | 470 | 515 | 490 |
| 剧烈反应的温度(℃) | 490 | 540 | 545 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作 | 现象 | 结论 |
| 分别打开瓶盖 | 其中一瓶瓶口上方产生白雾,另一瓶无明显变化 | 瓶口上方产生白雾的是浓盐酸,无明显变化的是浓硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com