
【题目】下图是对生成氯化钠反应关系的归纳与整理。
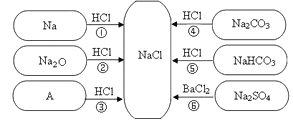
(1)物质A 是常见的碱,写出A 的化学式:_____________。
(2)反应④的类型为:____________ 。
(3)说出NaHCO3在医疗上的一种用途:___________________________ 。
(4)反应③、④、⑤、⑥能够进行的原因是___________________________ 。
(5)实验室配制200g 8 %的NaCl 溶液,需要水的质量是________g ,配制过程中为了加快NaCl 的溶解,可以采取的措施是___________________________ 。
【答案】 NaOH 复分解 治疗胃酸过多 有气体或沉淀或水生成 184g 用玻璃棒搅拌
【解析】(1)碱是指电离出的阴离子全部是氢氧根离子的化合物,A中含有钠元素又属于常见的碱,所以是氢氧化钠;
(2)反应④是碳酸钠与盐酸反应,相互交换成分,生成氯化钠和水和二氧化碳,故该反应为复分解反应;
(3)碳酸氢钠与盐酸反应生成氯化钠、水、二氧化碳,胃酸主要成分是盐酸,所以NaHCO3在医疗上的一种用途是可以治疗胃酸过多;
(4)反应③是碱与酸发生复分解反应有水生成、反应④⑤是盐与酸发生复分解反应有水和气体生成、反应⑥是盐与盐发生复分解反应有沉淀生成,复分解反应的条件是生成物中有沉淀、气体或水,反应③、④、⑤、⑥能够进行的原因是:有水或沉淀或气体产生;
(5)溶质质量=溶液质量×溶质的质量分数,配制200g 8%的NaCl溶液,需氯化钠的质量=200g×8%=16g;溶剂质量=溶液质量-溶质质量,则所需水的质量=200g-16g=184g,配制过程中为了加快NaCl的溶解,可用玻璃棒进行搅拌。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:初中化学 来源: 题型:
【题目】为了研究炼铁的主要反应原理,某化学兴趣小组的同学用一氧化碳还原氧化铁做实验。装置如下图所示。请回答下列问题:
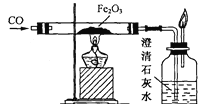
(1)在实验开始后可观察到如下现象:玻璃管中的粉末由_______色逐渐变为_______色,这说明了氧化铁在反应中失去了_______而被还原,这种粉末就是被还原出来的_______;澄清石灰水中出现_______,这说明一氧化碳夺取了氧化铁中的_______而被氧化,产生了_______气体。
(2)若一氧化碳是足量的,要制得56 g铁,至少需要氧化铁_______g,同时能产生二氧化碳_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请按照要求写出下列反应的化学方程式
(1)有二氧化碳生成的化合反应__________________________________________
(2)有二氧化碳生成的分解反应__________________________________________
(3)有二氧化碳参加的化合反应__________________________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:(1)水的密度为1.0g/mL.实验室配制50g溶质质量分数为5%的氯化钠溶液,需要称取氯化钠_____ g,需要量取水_____mL.
(2)配制的操作示意图如图,该实验的正确操作顺序为_____(填字母序号).
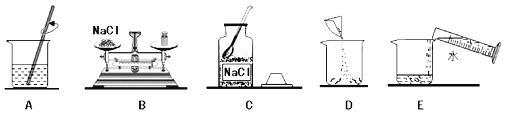
(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是_____
①氯化钠固体不纯 ②称量时,砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,有少量溶液洒出
A.①②③④ B.①③ C.①②③ D.①③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式能正确表示所述内容的是
A.铁片入到稀硫酸:2Fe+3H2SO4=Fe2(SO4)3 + 3H2↑
B.氢氧化钠变质:2NaOH + CO2 = Na2CO3 + H2O
C.实验室制备CO2:CaCO3 高温 CaO+CO2↑
D.铁丝在氧气中燃烧:4Fe + 3O2 点燃 2Fe2O3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】质量守恒定律的发现对化学的发展作出了巨大贡献.
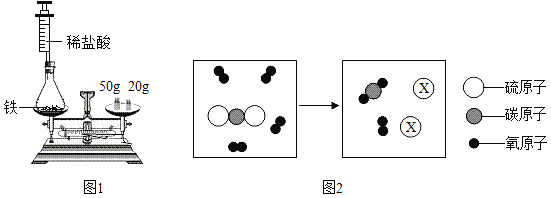
(1)为验证质量守恒定律,小华设计如图1所示装置进行实验.
实验时,先将装有药品的装置放在天平上,添加砝码,移动游码至天平平衡(如图1所示),然后取下装置,用针筒向锥形瓶中注入少量稀盐酸,反应后再将装置放置于天平上,观察到_____,从而验证了质量守恒定律.若将锥形瓶改为烧杯,则不能验证质量守恒定律,原因是_____.
(2)某反应的微观示意图如图2所示.
①X的化学式是_____.
②根据上述微观示意图,可得出化学反应遵循质量守恒定律的本质原因是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
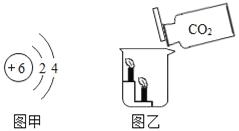
【题目】根据下列甲、乙图示和相关叙述,回答下列问题:
(1)图甲中该元素原子有_______个电子层,最外层有_______个电子.
(2)图乙所示的实验中,可以观察到______(选填“上层”或“下层”)蜡烛先熄灭,该实验都能得出CO2不能燃烧,也不支持燃烧,密度比空气______.
(3)最近,我国科学家宣布在南海成功开采可燃冰,成为世界上第一个能持续稳定开采可燃冰的国家,可燃冰外观像冰,它是在海底的高压、低温条件下形成的,它主要以甲烷水合物(CH48H2O)的形式存在,其中它的主要可燃成分是______(填化学式).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石灰石是生产玻璃、氯化钙等多种化工产品的原料。某研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
实 验 | 1 | 2 | 3 | 4 |
加入样品质量/g | 5 | 10 | 15 | 20 |
生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
(1)第几次反应中矿石有剩余?_________;
(2)表中m值是________;
(3)试计算这种石灰石中碳酸钙的质量分数为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com