
| ʵ�鲽�� | ʵ������ |
| ��ȡһ�����ĺϽ��ĩ���������������������Һ����ַ�Ӧ����ˣ���ֽ��ʣ���ﱸ�� | ��ĩ�����ܽ⣬������ɫ��ų� |
| ��ȡ��������ù������ʣ����������ϡ���ᣬ��ַ�Ӧ | �������ʲ����ܽ⣬������ɫ����ų�����Һ��dz��ɫ |
���� �������ܹ����������ƺ�ˮ��Ӧ����NaAlO2��һ�ֿ�ȼ�����壬���������غ㶨�ɿ�֪��������������������ϡ���ᷴӦ������dz��ɫ������������������ͭ������ϡ���ᷴӦ���з�����
��� �⣺��1��ȡһ�����ĺϽ��ĩ���������������������Һ����ַ�Ӧ����ˣ���ĩ�����ܽ⣬������ɫ��ų������ԺϽ��к�������ȡ��������ù������ʣ����������ϡ���ᣬ��ַ�Ӧ���������ʲ����ܽ⣬������ɫ����ų�����Һ��dz��ɫ�����ԺϽ��к�������ͭ���ۺϷ�����֪���Ͻ��к���Al��Fe��Cu��
��2�����з����ķ�Ӧ�������������ơ�ˮ��Ӧ����ƫ�����ƺ���������ѧ����ʽΪ��2Al+2H2O+2NaOH�T2NaAlO2+3H2����
��3�����з����ķ�Ӧ������ϡ���ᷴӦ����������������������ѧ����ʽΪ��Fe+H2SO4�TFeSO4+H2����
�ʴ�Ϊ����1��Al��Fe��Cu��
��2��2Al+2H2O+2NaOH�T2NaAlO2+3H2����
��3��Fe+H2SO4�TFeSO4+H2����
���� ������Ҫ�����˽����Ļ�ѧ���ʺͻ�ѧ����ʽ����д���ѶȲ���ע���ǿ���伴����ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ͻ���һ���н���Ԫ�� | B�� | ��������һ������Ԫ�� | ||
| C�� | �ᡢ����һ������Ԫ�� | D�� | ����һ���н���Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
| Ԫ�� | Na | Mg | �� | Si | P | �� | Cl |
| ԭ�ӵ����������� | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| ԭ�Ӱ뾶����10-10m�� | 1.86 | 1.60 | 1.43 | 1.17 | �� | 1.02 | 0.994 |
| ������� | +1 | +2 | �� | +4 | +5 | +6 | �� |
| ����� | -4 | �� | -2 | -1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
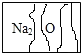 ʵ��������ƿ��ǩ�ܵ���ʴ����ͼ��ʾ������ɫ��Һ����ѧϰС�鿪չ̽����
ʵ��������ƿ��ǩ�ܵ���ʴ����ͼ��ʾ������ɫ��Һ����ѧϰС�鿪չ̽����| ʵ����� | ʵ������ |
| ��ȡ��������ɫ��Һ���Թ��У������μ�BaCl2��Һ �ھ��ú���ȥ�ϲ���Һ��������еμ�ϡ���� | ������ɫ���� �����������ݣ�������ʧ |
| ʵ����� | ʵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȼ�ŵ�ľ�����ֿ����������̼ | |
| B�� | ��ˮ�����������ƺ��Ȼ�� | |
| C�� | ���Ȼ�����Һ����̼������Һ����������Һ | |
| D�� | ������ͭ��Һ�����������ƺ��Ȼ�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
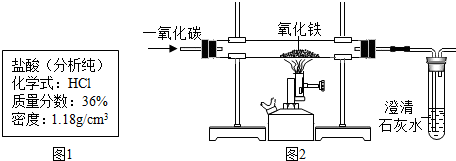
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com