
课堂上,老师取20g蔗糖放入不烧杯中,加少量水使它润湿,注入10mL浓硫酸,搅拌,同学们看到蔗糖先变黑后“发酵”形成“黑面包”,同时还闻到了刺激性气味,同学们判断黑色固体是碳,原因是浓硫酸具有强__________.
形成“黑面包”的主要原因是什么?在老师的指导下,同学们开展了探究活动.
(猜想与假设)浓硫酸与碳反应,生成大量气体使黑色固体膨胀.
(查阅资料)
Ⅰ.浓硫酸与碳在加热条件下反应,生成物中有SO2、CO2两种气体.
Ⅱ.SO2是一种具有刺激性气味的气体,能与Ca(OH)2溶液反应生成白色沉淀.
Ⅲ.SO2能使品红溶液褪色,而CO2不能.
(实验探究)
为验证碳与浓硫酸在加热条件下生成的气体产物,同学们在老师指导下设计并进行如图实验:

(事实与结论)
(1)请将能得出对应结论的实验现象填入表中.
验证气体 | 实验现象 | 实验结论 |
SO2 | __________ | 有SO2产生 |
CO2 | ___________ | 有CO2产生 |
(2)碳与浓硫酸反应的化学方程式是__________.
(3)浓硫酸与碳在加热条件下产生大量的SO2和CO2,使黑色固体膨胀,形成“黑面包”,猜想成立.
(反思与交流)
(1)小明同学提出,因老师的演示实验没有进行加热,所以同学们的探究实验无意义,其他同学一致否定了他的说法,理由是__________.
(2)若B、E中试剂交换,__________(填“能”或“不能”)得出有CO2产生的结论,理由是__________.
(3)C中酸性高锰酸钾溶液的作用是__________.
脱水性 B中品红溶液变红 D中品红溶液不变红,E中澄清石灰水变浑浊 C+2H2SO4(浓)CO2↑+2SO2↑+2H2O 浓硫酸溶于水放出大量的热 不能 SO2和CO2均能使E中澄清石灰水变浑浊,无法判断是否有CO2产生 吸收SO2,防止干扰CO2检验 【解析】浓硫酸有脱水性,能使蔗糖脱水生成C;【事实与结论】(1)浓硫酸与碳在加热条件下反应,生成物中有SO2、CO2两种气体.SO2能使品红...科目:初中化学 来源:江苏省南京市秦淮区2018届九年级二模化学试卷 题型:单选题
下列粒子结构示意图中,表示阴离子的是
A. 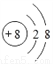 B.
B. 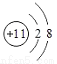 C.
C. 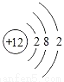 D.
D. 
查看答案和解析>>
科目:初中化学 来源:江苏省南京市玄武区2018届九年级中考第二次调研化学试卷 题型:单选题
我国对制碱工业作出重大贡献的科学家是( )
A. 徐光宪 B. 侯德榜 C. 张青莲 D. 戴安邦
B 【解析】制碱工业做出重大贡献的是侯德榜。徐光宪为我国“稀土之父”。张青莲主持测定 了铟、铱、锑、铕、铈、锗、锌、镝几种元素的相对原子质量新值,被国际原子量委员会采用为国际新标准。戴安邦是我国配位化学奠基人之一。查看答案和解析>>
科目:初中化学 来源:北京市朝阳区2018届九年级综合练习(二)化学试卷 题型:单选题
甲、乙两种固体物质的溶解度曲线如右图所示。下列说法正确的是

A. 乙的溶解度随温度的升高而增大
B. 相同温度时,甲的溶解度一定大于乙的溶解度
C. 将t1℃时甲的饱和溶液升温至t2℃,仍是饱和溶液
D. 分别将t1℃时甲、乙的饱和溶液升温至t2℃,所得溶液中溶质的质量分数相等
D 【解析】A. 甲的溶解度随温度的升高而增大,错误;B.t1℃、t2℃时,甲的溶解度等于乙的溶解度,错误;C. 将t1℃时甲的饱和溶液升温至t2℃,溶解度变大,变为不饱和溶液,错误;D. t1℃时,甲的溶解度等于乙的溶解度,则该温度时甲、乙的饱和溶液中溶质质量分数相等,分别将t1℃时甲、乙的饱和溶液升温至t2℃,溶解度增大,溶质质量分数不变,故所得溶液中溶质的质量分数相等,正确。故选D。 ...查看答案和解析>>
科目:初中化学 来源:北京市朝阳区2018届九年级综合练习(二)化学试卷 题型:单选题
下列符号中,表示2个氯原子的是
A. 2Cl B. 2Cl— C. Cl2 D. 2Cl2
A 【解析】元素符号前加数字表示原子个数,故选A。查看答案和解析>>
科目:初中化学 来源:专题15 科学探究(中考题)-决胜2018中考化学压轴题全揭秘精品 题型:科学探究题
碱式氯化镁【Mg(OH)Cl】受热能分解,它分解后产物是什么?小科进行了探究。
【猜想】Mg(OH)Cl分解后产物可能有:Mg、MgCl2、MgO、HCl气体、H2O、Cl2。
老师告诉他产物就是上述猪想中的其中几种,并提示Cl2是一种黄绿色有刺激性气味的气体。

【实验一】取少量的Mg(OH)Cl放入大试管中,按如图所示装置进行实验。加热过程中观察到足量硝酸银溶液中有白色沉淀产生,一段时间后,沉淀不再产生,大试管口也没有液滴形成,管内有固体剩余,无其他现象。由此推知Mg(OH)Cl分解后产物中有_______气体,无其他气体。
【实验二】取少量实验一的剩刹余固体于试管中,加入足量稀盐酸,没有气泡产生。由此推知Mg(OH)Cl分解后产物中没有_______。
【实验三】再取少量实验一的剩余固体,加入足量稀硝酸,固体全部溶解,再滴入AgNO3溶液,无沉淀产生。由此推知Mg(OH)Cl分解后产物中没有________。
【结论】Mg(OH)Cl受热分解的化学反应方程式为____________。
【实验一】HCl 【实验二】Mg 【实验三】MgCl2 【结论】Mg(OH)ClMgO+HCl↑ 【解析】【实验一】管内无黄绿色气体,说明没有生成氯气;大试管口也没有液滴形成,说明没有生成水;硝酸银溶液中有白色沉淀产生,说明生成了HCl气体,HCl气体溶于水形成盐酸,盐酸与硝酸银反应生成氯化银沉淀;【实验二】镁能与稀盐酸反应生成氢气,猜想中的其他物质不能。现取少量实验一的剩刹余固体于试...查看答案和解析>>
科目:初中化学 来源:黑龙江省绥化市绥棱县2018届九年级(五四学制)下学期第六次月考化学试卷 题型:填空题
阅读下面的科普短文,回答问题:
同学们一定见过晶莹剔透的水晶,你知道它的成分吗?其实水晶的主要成分是二氧化硅(SiO2),二氧化硅是一种无色晶体,熔点很高,硬度很大,不溶于水,常温下二氧化硅能与强碱溶液缓慢反应.SiO2在高温条件下能与CaO反应生成CaSiO3,二氧化硅不与水反应,也不与一般的酸反应,却可以与氢氟酸反应,玻璃中含有二氧化硅。
(1)写出二氧化硅的物理性质____________________________(答出一点);
(2)用氢氟酸将精美的图案刻蚀在玻璃上,该过程属于_______________变化(填“物理”或“化学”);
(3)二氧化硅与氢氧化钠反应的化学方程式为 _______________________,因此实验室中储存氢氧化钠溶液的试剂瓶应用___________________(填“玻璃塞”或“橡胶塞”)
无色晶体(或熔点高、硬度大、不溶于水) 化学 SiO2+2NaOH=Na2SiO3+H2O 橡胶塞 【解析】(1)必须经化学变化才能表现的性质叫化学性质,不需要发生化学变化就能表现的性质叫物理性质。二氧化硅的物理性质: 无色晶体,熔点很高,硬度很大,不溶于水; (2)物理变化和化学变化的根本区别在于是否有新物质生成,如果有新物质生成,则属于化学变化; 反之,则是物理变化。用氢氟酸将精美的图案...查看答案和解析>>
科目:初中化学 来源:黑龙江省绥化市绥棱县2018届九年级(五四学制)下学期第六次月考化学试卷 题型:单选题
下列物质间不能发生复分解反应的是( )
A.碳酸钠溶液和氯化钙溶液 B.氢氧化钠溶液和氯化钾溶液
C.碳酸钾溶液和盐酸 D.硫酸铜溶液和氯化钡溶液
B 【解析】 试题分析:A、碳酸钠溶液和氯化钙溶液相互交换成分生成碳酸钙沉淀和氯化钠,能发生复分解反应,故选项错误。B、氢氧化钠溶液和氯化钾溶液相互交换成分没有沉淀、气体或水生成,不能发生复分解反应,故选项正确。C、碳酸钾溶液和盐酸相互交换成分生成氯化钾、水和二氧化碳,能发生复分解反应,故选项错误。D、硫酸铜溶液和氯化钡溶液相互交换成分生成硫酸钡淀和氯化铜,能发生复分解反应,故选项错误...查看答案和解析>>
科目:初中化学 来源:山东省商河县2018届中考二模(5月)化学试卷 题型:单选题
化学兴趣小组在做稀盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化,其图像如图所示,下列说法正确的是( )
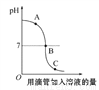
A. 向图中A点所示溶液滴入酚酞试液,溶液不变色
B. 该实验是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的烧杯中
C. 图中C点所示溶液中,含有溶质NaCl和NaOH
D. 由A点到B点的pH变化过程证明酸和碱发生了中和反应
D 【解析】A、图中A点所示溶液pH大于7,呈碱性,滴入酚酞试液,溶液变红,错误; B、图象中pH值的变化是从大于7逐渐的减小到小于7,可知原溶液显碱性,然后不断的加入酸性溶液,使pH减小,说明是把稀盐酸滴加到氢氧化钠溶液中,正确;C、图中C点所示溶液中,盐酸过量,故溶液中含有的溶质为NaCl和HCl,错误;D、由A点到B点的pH变化过程,碱性逐渐变弱,说明酸和碱发生了中和反应,正确。...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com