
【题目】下列实验目的、操作、现象、结论都正确的是
选项 | 实验目的 | 实验操作 | 实验现象 | 实验结论 |
A | 测溶液pH | 用玻璃棒蘸取待测液滴在用蒸馏水润湿的pH试纸上 | 试纸变为浅红色 | 溶液pH为2 |
B | 鉴别NaOH和NH4NO3 | 在装有等量水的试管中分别加入a、b固体 | 加a的试管水温升高,加b的试管水温降低 | a是NaOH b是NH4NO3 |
C | 验证燃烧是否需要O2 |
| 前者不燃烧,后者燃烧 | 燃烧需要O2 |
D | 比较Al、Cu的活泼性 | 将未经打磨的Al条放入CuSO4溶液中 | 无明显现象 | 活泼性Al<Cu |
A. A B. B C. C D. D
科目:初中化学 来源: 题型:
【题目】已知某固体样品A可能含有Na2SO4、BaCl2、CuSO4、KCl四种物质中的一种或多种,按下图所示进行探究实验,出现的现象如图中所述(设计过程中所有发生的反应都恰好完全反应)。试根据实验过程和发生的现象,填写以下空白:
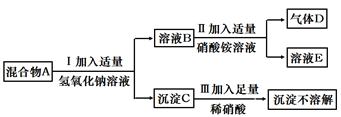
(1)沉淀C的化学式为__________,沉淀颜色为__________(“酸性”,“中性”,“成性”)。
(2)将气体D通入水中,其水溶液呈_______________。
(3)溶液E中,一定存在的阳离子是_________(填写离子符号)。
(4)写出步聚Ⅱ中生成气体D的化学方程式:______________________________。
(5)固体样品A中,还不能确定的物质是_________(填写化学式)。
(6)固体样品A中,一定不存在的物质是__________ (填写化学式),得出此结论不的理由是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
“菠菜豆腐”是我国的传统菜肴,近年来,有关“菠菜豆腐”的争论主要集中在钙吸收率方面。菠菜中富含易溶于水的草酸,若单独吃菠菜,其中的草酸会结合胃内食糜中的部分铁和锌,还能够进入血液,沉淀血液中所含的钙。而将豆腐与菠菜同食,豆腐中的可溶性钙与菠菜中的草酸结合成不溶性的草酸钙(CaC2O4)沉淀,既能够保护食物中的铁和锌等元素,还能保证人体内的钙不被草酸结合。因此,豆腐与菠菜同食仍不失为一个好的搭配。
研究人员以新鲜菠菜和新鲜豆腐为材料,进行了“菠菜豆腐”烹调方法的研究。
(实验1)探究菠菜质量对菜肴中可溶性钙含量的影响。实验结果如下:
豆腐/ g | 10 | 10 | 10 | 10 | 10 |
菠菜/ g | 5 | 10 | 15 | 20 | 25 |
可溶性钙/总钙 | 0.364 | 0.287 | 0.186 | 0.125 | 0.088 |
(实验2)探究菠菜焯水时间对菜肴中可溶性钙含量的影响。
用100g豆腐和250g菠菜(焯水时间不同)制成菜肴,测定每100g“菠菜豆腐”中可溶性钙的质量,结果见下图。

以上研究表明,烹调“菠菜豆腐”时,如能适当减少菠菜的比例,并预先将菠菜焯水,则豆腐中钙的吸收率将会显著提高。
根据文章内容,回答下列问题:
(1)可溶性钙中的“钙”是指_________(“钙单质”或“钙元素”)。
(2)豆腐中富含的营养素是_____________。
A. 维生素 B. 糖类 C. 蛋白质 D. 油脂
(3)结合实验1的数据分析,可得到的结论是_________________。
(4)用焯水后的菠菜制作“菠菜豆腐”,能提高可溶性钙含量的原因是__________。
(5)草酸钙在高温下完全分解可得到两种气态氧化物和一种固态氧化物,该反应的化学方程式为____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒在元素周期表中的某些信息如图,下列说法不正确的是
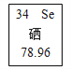
A. 硒属于金属元素 B. 硒的原子序数是34
C. 硒原子中的质子数是34 D. 硒的相对原子质量是78.96
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图中A~J表示初中化学常见的物质。其中B、C、F、J为氧化物,且C能造成煤气中毒,F中两种元素的质量比是4∶1;D、H为相同类别的化合物,E、I也为相同类别的化合物,且D、I在某些情况下可用作干燥剂。“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物和生成物已略去。
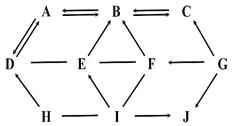
(1)写出化学式:C________________。
(2)写出化学方程式:
A转化为D的反应________________________________;
I转化为E的反应________________________________;
F转化为B的置换反应____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下图回答问题:
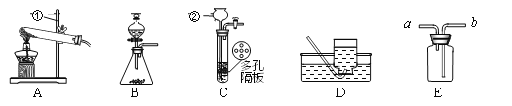
(1)仪器名称:①________,②______。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置______(选填序号)和D组合,反应的化学方程式为________,二氧化锰的作用是_______。
(3)实验室可用装置B或C制H2,C装置相对于B的优点有__________。用E装置收集H2,气体应从________(选填“a”或“b”)端通入。
(4)有同学将实验室制得的CO2通入澄清石灰水,石灰水未变浑浊,于是作如右图探究:

①实验室制CO2反应的化学方程式_________。
②装置F、H中溶液变浑浊,G中溶液不变浑浊,则原石灰水未变浑浊的原因是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据所示的实验或装置,回答问题:
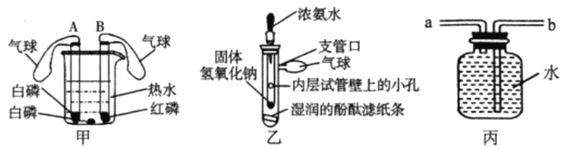
(1)甲实验的目的是:_______________________。
(2)乙实验中,向内层试管内滴入少量浓氨水后,湿润的酚酞滤纸条处出现的现象是_____________。实验中氢氧化钠固体的作用是________________________。
(3)丙装置在化学实验中具有广泛的用途,俗称“万能瓶”,若用该装置收集氧气,气体应从装置的__________端进入(选填“a”或“b”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】鸡蛋主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3,里面覆盖一层蛋壳膜。化学活动兴趣小组的同学开展了以下探究活动:
(提出问题)蛋壳中的CaCO3含量是多少?
(查阅资料)
a、蛋壳经过科学检测其中含CaCO3的质量分数约为82%~85%,含蛋白质质量分数约14-17%。
b、蛋壳膜中蛋白质含量约为90%~93%。
(设计方案)
方案一:用“灼烧法”,将该蛋壳放在空气中充分灼烧并采集相关数据进行测定。
方案二:用“酸处理法”,将蛋壳与稀盐酸反应进行测量处理。
(进行实验)
方案一:称取12.0 g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16 g。
方案二:用如图所示的实验装置,称取12 g蛋壳样品进行实验(假设其他成分均不与HCl反应,装置内试剂均足量。)
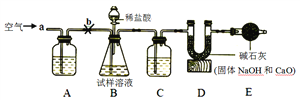
(实验步骤)
① 按如图连接好装置后,并检查装置的气密性;
②向B装置中加入蛋壳样品后,先通入一会儿空气;
③称量装置D及其中药品的质量;向蛋壳样品中滴入5%的稀盐酸,直到________为止;
④再缓缓通入空气一会儿,至装置D中质量不再增加为止;⑤称量装置D及其中药品的质量。
(数据处理)
方案一:该小组同学认为固体减少为分解产生的二氧化碳质量,据此求出蛋壳中CaCO3的质量分数为91.7%
方案二:测得反应后D装置及其中药品的总质量增加了4.4g,样品中碳酸钙的质量分数是多少________? (写出计算过程,计算结果精确到0.1%)
(评价反思)
(1)方案一:发生分解反应的化学方程式为________,测定值与科学检测的数据有较大误差,主要原因是________。
(2)方案二:装置A中的化学方程式为________,如装置C中的药品为浓硫酸,其作用是________,装置E的作用是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铜跟稀硝酸可发生反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。现有4.8g的铜与100g的稀硝酸恰好完全反应。
(1)根据化学方程式计算反应生成的一氧化氮质量为多少__________?
(2)求反应后溶液的溶质质量分数___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com