
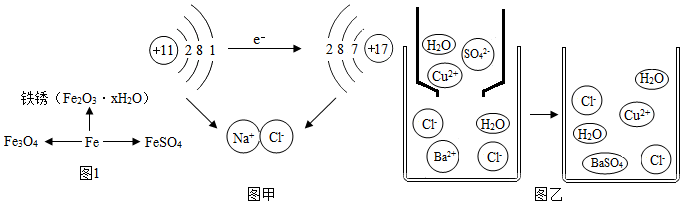

分析 (1)①根据铁和氧气在点燃的条件下生成四氧化三铁,放出大量的热进行分析;
②根据铁制品的锈蚀过程,实际上是铁与空气中的氧气和水等发生化学反应的过程进行分析;
③根据化合价代数和为零进行分析;
(2)①根据物质的化学性质与原子的最外层电子数有关进行分析;
②根据硫酸铜和氯化钡反应生成硫酸钡沉淀和氯化铜进行分析;
(3)①根据升高温度可以加快分子的运动速率进行分析;
②根据物质燃烧的条件进行分析;
③根据在金属活动性顺序中,只有排在氢前的金属才可以和稀酸溶液反应生成氢气,而且越靠前的金属活动性就越强,和稀酸溶液反应时现象就越剧烈进行分析.
解答 解:(1)①铁和氧气在点燃的条件下生成四氧化三铁,放出大量的热;
②铁制品的锈蚀过程,实际上是铁与空气中的氧气和水等发生化学反应的过程;
③在FeSO4中硫酸根离子显示-2价,亚铁离子显示+2价,所以与铁元素化合价相同的铁的氧化物的化学式是FeO;
(2)①图甲是钠与氯气反应生成氯化钠的示意图,该图说明在化学反应过程中,原子核不变,电子层数可能变化,原子在发生化学变化时,通过得失电子形成化合物,所以一定发生变化的是b;
②硫酸铜和氯化钡反应生成硫酸钡沉淀和氯化铜,所以从粒子角度分析该化学反应能发生的原因是:钡离子和硫酸根离子结合生成难溶于水硫酸钡沉淀;
(3)①升高温度可以加快分子的运动速率,所以实验1中同时向烧杯中加入一粒相同大小的品红,发现整杯水变红的时间热水比冷水短,这是因为:受热的情况下,分子能量增大,运动速率加快;
②白磷的着火点低,先燃烧,红磷的着火点高,后燃烧,所以实验2中使用铜片是为了对比可燃物的着火点不同;
③在金属活动性顺序中,只有排在氢前的金属才可以和稀酸溶液反应生成氢气,而且越靠前的金属活动性就越强,和稀酸溶液反应时现象就越剧烈,所以
a.铜不能发生酸发生反应,铜可以将硝酸银中的银置换出来,所以不能说铜不会发生置换反应,故错误;
b.镁表面的气泡产生最剧烈,所以四种金属中金属活动性最强的是Mg,故正确;
c.每65份质量的锌会生成2份质量的氢气,每56份质量的铁会生成2份质量的氢气,所以等质量的锌和铁分别与足量的盐酸发生生成气体质量:Zn比Fe少,故错误.
故选:ac.
故答案为:(1)①放出;
②氧气和水;
③FeO;
(2)①b;
②钡离子和硫酸根离子结合生成难溶于水硫酸钡沉淀;
(3)①受热的情况下,分子能量增大,运动速率加快;
②可燃物的着火点;
③ac.
点评 本题主要考查了金属的化学性质、燃烧的条件等方面的知识,难度不大,需要在平时的学习中加强记忆即可完成.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 红磷在空气中燃烧产生大量白烟 | |
| D. | 木炭在氧气中燃烧,发出黄色火焰,生成有刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 反应属于氧化反应 | |
| B. | X的化学式是Ag2S | |
| C. | 反应前后元素的种类不变 | |
| D. | 反应前后所有元素的化合价都发生了变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧离子的结构示意图为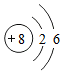 | |
| B. | H2O和H2O2中氢元素的化合价相同 | |
| C. | 水和冰块混合形成混合物 | |
| D. | 水沸腾时可冲起壶盖,说明温度升高水分子变大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
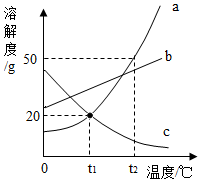 如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )| A. | 随温度升高,a、b、c三种物质的溶解度均增大 | |
| B. | t2℃时,把50g a放入50g水中,可得到100g a的饱和溶液 | |
| C. | 将t2℃时等质量的a、b饱和溶液降温到t1℃,析出晶体的质量a小于b | |
| D. | t1℃时,a、c的溶解度相等,则两饱和溶液的溶质质量分数也相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com