
分析 (1)根据铁元素与人体健康之间的关系分析回答.
(2)根据在化合物中正负化合价代数和为零,结合高铁酸钠(Na2FeO4)的化学式进行解答本题.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物的化学式;
(4)根据金属的性质来分析.
解答 解:(1)铁是血红蛋白的成分,在酱油中加入铁强化剂,是我国为解决贫血而实施的项目.故填:贫血;
(2)钠元素显+1价,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6.故填:+6;
(3)根据反应的化学方程式,设未知反应物的化学式为X,应物中铁、氧、氢原子个数分别为4、10、8,反应后的生成物中铁、氧、氢原子个数分别为4、12、12,根据反应前后原子种类、数目不变,则2X含有2个氧原子和4个氢原子,则每个X子由1个氧原子和2个氢原子构成,则物质X的化学式为H2O.故填:H2O;
(4)铁具有导电性,能将静电导入地下,故填:能导电.
点评 本题难度不大,掌握微量元素的生理功能和缺乏症、利用化合价的原则计算指定元素的化合价的方法、原子守恒来确定物质的化学式等即可正确解答本题.


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:初中化学 来源: 题型:选择题
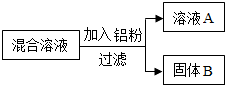 某同学用一定量Cu(NO3)2和Zn(NO3)2的混合溶液进行了如图实验,则对溶液甲和固体乙成分的描述正确的是( )
某同学用一定量Cu(NO3)2和Zn(NO3)2的混合溶液进行了如图实验,则对溶液甲和固体乙成分的描述正确的是( )| A. | 溶液甲中一定有Zn(NO3)2和Al(NO3)3 | B. | 溶液乙中一定有Cu(NO3)2和Al(NO3)3 | ||
| C. | 固体乙中一定有Cu,可能有Zn和Al | D. | 固体乙中一定有Cu和Zn,可能有Al |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 西达苯胺由五种元素组成 | B. | 西达苯胺是一种有机高分子化合物 | ||
| C. | 一个西达苯胺分子由48个原子构成 | D. | 西达苯胺中氮、氧元素质量比是7:4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Y<X<Z | B. | Z<Y<X | C. | X<Y<Z | D. | Z<X<Y |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 滤液N中一定存在Zn2+ | B. | 滤液M的颜色呈蓝色 | ||
| C. | 滤渣N中一定含有Zn、Fe和Cu | D. | 滤渣N的质量小于加入锌粉的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
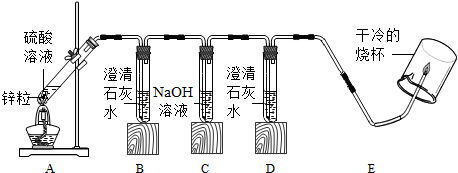
| A中硫酸的 质量分数 | 实验现象 | |||
| B中 | D中 | E处 | ||
| 实验一 | 98% | 变浑浊 | 不变浑浊 | 不可燃 |
| 实验二 | 50% | 稍变浑浊 | 不变浑浊 | 可燃 |
| 实验三 | 25% | 不变浑浊 | 不变浑浊 | 可燃 |
 ”中填写计量数,在“SO2”上填写化学式):
”中填写计量数,在“SO2”上填写化学式):
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com