
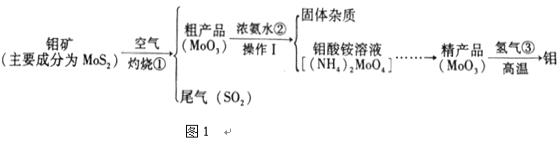
钼具有高强度、高熔点、而腐蚀等优点,在工业上得到广泛的利用。图1是化工生产中制备金属钼的部分流程图(假设杂质不与空气反应)。
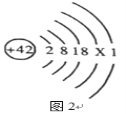
(1)钼是人体及动植物必需的_______________(选填“微量元素”或“常量元素”),原子的结构示意图2,其中X是_________________。
(2)步骤①反应的化学方程式_________________________________。
(3)下列物质可以用来吸收SO2尾气的是_________(填字母)。
A 氢氧化钠溶液 B 浓硫酸 C 氨水
(4)(NH4)2MoO4中Mo的化合价是_____________,在农业上既是钼肥又是_______肥。
(5)如果在实验室模拟操作Ⅰ,则需要使用的主要玻璃仪器有漏斗、玻璃棒、________。
(6)利用H2和CO分别还原等质量的精产品(MoO3),所需的还原剂的质量比为____。
科目:初中化学 来源:湖南省长沙市岳麓区长郡教育集团2019-2020学年九年级上学期第三次月考化学试卷 题型:实验题
认识反应规律,控制反应条件,让化学反应为人类服务。化学小组的同学利用如图所示的装置探究燃烧的条件。小明同学对以上实验进行概括,得出的下列说法中,不正确的是_____(填字母代号)。
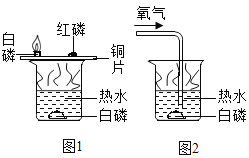
A 此组实验烧杯中的热水只起提高温度的作用
B 图1中水下白磷未燃烧是由于没有与氧气接触
C 图1实验对环境无影响
D 若将图2中白磷换成红磷,不能观察到燃烧现象
查看答案和解析>>
科目:初中化学 来源:山西省太原市2019-2020学年九年级上学期12月月考化学试卷 题型:单选题
如图是 元素周期表的一部分,下列说法错误的是( )
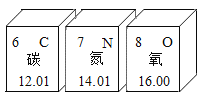
A.氧的相对原子质量是16.00
B.碳原子最外层有6个电子
C.原子序数等于7的是氮元素,属于非金属元素
D.一种元素可以形成多种单质
查看答案和解析>>
科目:初中化学 来源:安徽省沿淮教育联盟2019-2020学年九年级上学期第三次月考化学试卷 题型:单选题
推理是常用的学习方法,下列推理正确的是
A.分子、原子都是不带电的粒子,所以不带电的粒子一定是分子或原子
B.木炭、活性炭可用于净化空气,所以碳单质都能净化空气
C.化学反应前后原子总数不变,所以化学反应前后分子总数也不变
D.点燃可燃性气体前要验纯,所以点燃氢气前一定要验纯
查看答案和解析>>
科目:初中化学 来源:福建省莆田市2019届九年级质检化学试卷 题型:计算题
碱式硫酸铁常用于污水处理。可用铁锈与稀硫酸制取:Fe2O3 + 2H2SO4 == 2Fe(OH)SO4 + H2O。制备100.0kg碱式硫酸铁需消耗30%稀硫酸的质量是多少?________________
查看答案和解析>>
科目:初中化学 来源:福建省莆田市2019届九年级质检化学试卷 题型:单选题
下列常见金属的活动性顺序中,关于X、Y、Z三种金属的推测正确的是( )
K Ca Na X Al Zn Y Sn Pb (H) Z Hg Ag Pt Au
A. X、Y、Z都能与稀硫酸发生反应
B. X、Y、Z对应的金属可能是Mg、Fe、Cu
C. X、Y、Z三种金属元素都位于元素周期表的第三周期
D. 常温下,X、Y、Z都能将AgCl中的Ag置换出来
查看答案和解析>>
科目:初中化学 来源:河南省驻马店市2019届中考化学一模试卷 题型:单选题
食盐不仅可以做调味品,还是一种重要的化工原料。电解饱和食盐水,不可能得到的产物是( )
A. H2 B. Cl2
C. NaOH D. Na2CO3
查看答案和解析>>
科目:初中化学 来源:江苏省2019届九年级下学期第二次模拟考试化学试卷 题型:实验题
据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。同学们对废旧手机中的金属回收产生兴趣。
(提出问题)
从废旧手机中可以回收到哪些有价值的金属?如何回收?

(查阅资料)
Ⅰ.手机电路板中的金属及其价格如下表所示:
种类 | Fe | Cu | Al | Ni | Au | Ag | Pd(钯) |
市场价格/($/t) | 365 | 7175.5 | 1710.5 | 14235 | 4.7×107 | 7.6×105 | 2.7×107 |
矿石中含量 | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
手机电路板中含量 | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
说明:Fe、Cu、Al、Ni的含量用质量分数(%)表示,Au、Ag、Pd的含量的单位为“g/t”。
Ⅱ.Ni的金属活动性位于氢前;Pd的金属活动性位于氢后;NiCl2溶液为绿色。
(实验方案)
第一步:选择值得回收的金属。
依据资料Ⅰ中的数据,废旧手机中有回收价值的金属有Au、Ag、Cu、Pd,
(1)原因是:①它们的市场价格较高;②_____。
第二步:设计实验分离、回收部分金属。
序号 | 实验步骤 | 实验现象 |
Ⅰ | 取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出 | 焊锡熔化 |
Ⅱ | 将金属电路放入烧杯中,加入过量10%的稀盐酸浸泡 | …… |
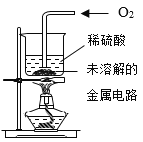
Ⅲ | 取Ⅱ中未溶解的金属电路,用蒸馏水洗净后,放入如上图所示装置中,进行实验。 | 溶液逐渐变成蓝色,仍有微量金属固体未溶解 |
Ⅳ | 过滤Ⅲ中烧杯中的物质,洗涤滤纸上的物质 | 滤纸上仍有微量金属固体 |
(问题讨论)
(2)由步骤I中的现象,可推知的焊锡的物理性质是_____(填字母)。
a.熔点低 b.硬度大 c.抗腐蚀性强
(3)步骤Ⅱ中实验室用溶质质量分数为37%、密度是1.18g•mL-1的浓盐酸配制10%的盐酸185g,需要浓盐酸_____ml;配制该稀盐酸应选择的量筒量程(水的密度为1g/cm3)为_____(填字母)。
a.10ml b.50ml c.100ml d.200ml
(4)步骤Ⅱ所得溶液中,至少含有_____(填数字)种溶质,该步骤中对应的实验现象是_____。
(5)请写出步骤Ⅲ中,溶液变成蓝色的化学方程式_____。
(6)步骤Ⅳ中过滤操作用到的玻璃仪器有玻璃棒、_____和_____,其中玻璃棒的作用是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com